El autor declara que no tiene conflictos de intereses en relación con el tema abordado en este documento.
José Galbe Sánchez-Ventura. Prevención y cribado de la enfermedad celíaca. En: Recomendaciones PrevInfad / PAPPS [en línea]. Actualizado abril 2025. [consultado DD-MM-AAAA]. Disponible en: https://previnfad.aepap.org/monografia/celiaca
INTRODUCCIÓN
La enfermedad celíaca (EC) es una intolerancia permanente a la fracción proteínica del gluten que produce daño en la mucosa del intestino delgado proximal. Se presenta en individuos genéticamente predispuestos. El diagnóstico se basa en la histopatología de la mucosa intestinal, aunque actualmente se admite como criterio diagnóstico una elevación de los marcadores serológicos diez veces superior el límite superior de la normalidad (1–9).
MAGNITUD DEL PROBLEMA
La prevalencia de EC (PREC) en diferentes países y áreas geográficas ha aumentado en los últimos años debido, en parte, a la utilización generalizada de marcadores serológicos que han permitido conocer la existencia de formas latentes y silentes de EC. Los principales marcadores son los anticuerpos antiendomisio (EMA), antitransglutaminasa tisular (tTGA), antigliadina (AGA) y la inmunoglobulina A (IgA) frente a péptidos deaminados (DGP-IgG) (1–4,8,10–14). En España, la PREC oscila entre 1:357 para la población adulta y 1:71 en la infancia (4). Hay una mayor PREC en las mujeres con una correlación 2:1. Diferentes investigadores informan de una PREC parecida en todas las regiones del mundo, en torno al 1% (1–3). En Italia la PREC es de 1,34%. En el caso de los niños saharauis es alrededor del 5% (15). La PREC ha aumentado en los últimos años y se especula como posibles causas el aumento de consumo de gluten y su globalización, así como la mejoría y sencillez de los métodos diagnósticos y una mayor alerta sobre EC por parte de los médicos.
Se puede ver la prevalencia de EC en distintas situaciones en las tablas 3 y 4.
MARCO ANALÍTICO
Utilizaremos el marco analítico de la USPSTF para la formulación de las preguntas clínicas (figura 1). Para las recomendaciones utilizaremos el sistema GRADE. Tras exponer el marco analítico, en las tablas 1 y 2 se pueden ver las preguntas clínicas derivadas del mismo (16–21).
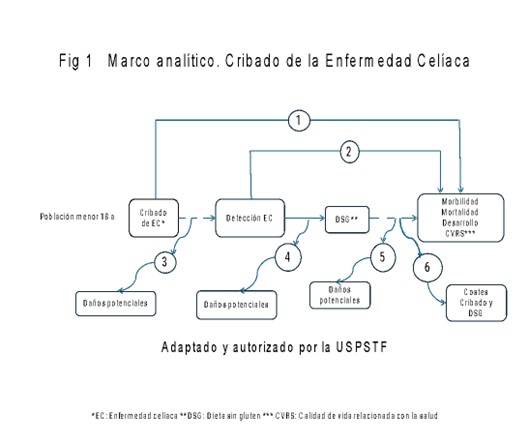
PREGUNTAS CLÍNICAS (tablas 1 y 2)
Tabla 1. Preguntas Clínicas
|
1.- ¿El cribado de EC en menores de 18 años ¿mejora la morbi-mortalidad,la calidad de vida o el trastorno de desarrollo causado por la misma
|
|
2.- ¿La detección precoz de EC en menores de 18 años ¿mejora la morbi-mortalidad, la calidad de vida o el trastorno de desarrollo causado por la misma?
|
|
3.- ¿Cuáles son los daños potenciales derivados del cribado de la EC?
|
|
4.- ¿Cuáles son los daños potenciales de la detección precoz de EC?
|
|
5.- ¿Cuáles son los daños derivados de la dieta sin gluten (DSG)?
|
|
6.- ¿Cuáles son los costes del cribado y de la DSG?
|
Tabla 2. Preguntas Clínicas relacionadas
|
7.- ¿Cuál es la adherencia a la DSG en los pacientes diagnosticados de EC?
|
|
8- ¿La introducción del gluten en la dieta en mayor cantidad diaria o en una determinada edad influye en el desarrollo posterior de EC?
|
|
9- ¿La introducción del gluten durante la lactancia materna disminuye la probabilidad de desarrollo posterior de EC?
|
PREGUNTAS CLÍNICAS
Pregunta 1.- ¿El cribado de la EC (CC) en menores de 18 años mejora la morbi-mortalidad, la calidad de vida o el trastorno de desarrollo causado por la misma?
No existen pruebas de calidad que evalúen el efecto directo del CC sobre la morbilidad, mortalidad, desarrollo o calidad de vida. Las respuestas hay que buscarlas en los demás puntos de la cadena causal tal y cómo se muestra en la Fig 1 del marco analítico.
Pregunta 2.- ¿La detección precoz de EC en menores de 18 años mejora la morbi-mortalidad, la calidad de vida o el trastorno de desarrollo causado por la misma?
Según los criterios de la ESPGHAN el diagnóstico definitivo requiere la práctica de una biopsia intestinal o que los marcadores serológicos superen 10 veces el límite superior de la normalidad (1–4,22–27).
Anticuerpos antigliadina (AGA). Fueron los primeros en utilizarse. Son de clase tanto IgA como IgG, pero se utilizan preferentemente los de tipo IgA. Su eficacia para el CC es mayor en niños que en adultos (tablas 3 y 4). Existe una extensa bibliografía que estudia la eficacia de los test diagnósticos (1–4,24–26,28).
Anticuerpos antitransglutaminasa 2 (tTGA) por el método ELISA (24,29,30). La transglutaminasa, una enzima que se libera tras el daño tisular. Se determina por ELISA. Los tTGA se han mostrado como el marcador más útil y hoy en día. Para mejorar la sensibilidad del cribado es importante determinar simultáneamente la IgA total, ya que al ser estos anticuerpos de tipo IgA, pueden darse falsos negativos para cribado de EC si existe un déficit asociado de esta inmunoglobulina (1–4). En las tablas 3, 4 y 5 puede apreciarse la eficacia de las pruebas diagnósticas, tanto en población general como de riesgo. En las tablas se especifican las poblaciones en las que debe realizarse el CC al tener un mayor riesgo de presentar EC. También existe consenso en combinar la determinación de tTGA con la de HLA DQ2/DQ8 que tienen un alto valor predictivo negativo (VPN) como veremos en el siguiente apartado (1–3,25,26,29–35) (tabla 5).
Tabla 3. Rendimiento del test t Transglutaminasa (tTgA) IgA. Se: 98%. Es: 70%.
|
Población
|
Prevalencia de EC
|
VPP
|
VPN
|
|
Gral
|
1,00%
|
3,20%
|
100,00%
|
|
Fam 1º
|
6,00%
|
17,30%
|
99,80%
|
|
Fam 2º
|
2,50%
|
7,70%
|
99,90%
|
|
Anemia
|
10,00%
|
26,60%
|
99,70%
|
|
Baja talla
|
10,00%
|
26,60%
|
99,70%
|
|
S Down
|
10,00%
|
26,60%
|
99,70%
|
|
Diabetes 1
|
8,00%
|
22,10%
|
99,80%
|
|
Autoinmunes
|
6,00%
|
17,30%
|
99,80%
|
|
S Turner
|
6,00%
|
17,30%
|
99,80%
|
|
S Williams
|
8,00%
|
22,10%
|
99,88%
|
VPP: Valor predictivo positivo
VPN: Valor predictivo negativo
Tabla 4. Rendimiento del test Ac antiendomisio IgA. Se: 95%. Es: 94%.
|
Población
|
Prevalencia de EC
|
VPP
|
VPN
|
|
Gral
|
1,00%
|
13,80%
|
99,60%
|
|
Fam 1º
|
6,00%
|
50,00%
|
99,70%
|
|
Fam 2º
|
2,50%
|
28,90%
|
99,90%
|
|
Anemia
|
10,00%
|
63,80%
|
99,40%
|
|
Baja talla
|
10,00%
|
63,80%
|
99,40%
|
|
S Down
|
10,00%
|
63,80%
|
99,40%
|
|
Diabetes 1
|
8,00%
|
57,90%
|
99,50%
|
|
Autoinmunes
|
6,00%
|
50,00%
|
99,70%
|
|
S Turner
|
6,00%
|
50,00%
|
99,70%
|
|
S Williams
|
8,00%
|
57,90%
|
99,50%
|
VPP: Valor predictivo positivo
VPN: Valor predictivo negativo
Tabla 5. Rendimiento del test HLA DQ2/DQ8. Se: 99%. Es:56%
|
Población
|
Prevalencia de EC
|
VPP
|
VPN
|
|
Gral
|
1,00%
|
2,20%
|
100
|
|
Fam 1º
|
6,00%
|
12,60%
|
99,90%
|
|
Fam 2º
|
2,50%
|
5,50%
|
100,00%
|
|
Anemia
|
10,00%
|
20,00%
|
99,90%
|
|
Baja talla
|
10,00%
|
20,00%
|
99,90%
|
|
S Down
|
10,00%
|
20,00%
|
99,90%
|
|
Diabetes 1
|
8,00%
|
16,40%
|
99,80%
|
|
Autoinmunes
|
6,00%
|
9,90%
|
56.00%
|
|
S Turner
|
6,00%
|
9,90%
|
99,90%
|
|
S Williams
|
8,00%
|
16,40%
|
99,80%
|
VPP: Valor predictivo positivo
VPN: Valor predictivo negativo
También puede determinarse la tGA por el método Radio Binding Assay (RBA). Con una precisión muy parecida a los anteriores.
Otro método es la IgA antigliadina, realizada de forma rápida en la propia consulta (POC test, BIOCARD). Esta prueba está diseñada para ser realizada de forma rápida y autónoma por la propia familia sin necesidad de que lo realice un profesional (35-37).
Otros test son todavía menos invasivos, se basan en muestras de saliva, pero su eficacia no está todavía bien establecida y no están disponibles en nuestro medio (35-37).
Un trabajo español de 2024 señala que sobre una serie de 184 casos de pacientes diagnosticados de EC mediante biopsia, encuentran hasta un 19,1% de casos mal clasificados de EC cuando se utiliza la técnica de tTGA por quimioluminiscencia, uno de los métodos más comúnmente usados. Esta situación se produce especialmente en casos de infección por H. Pylori y con menos frecuencia G. Lamblia y Rotavirus. Estos autores proponen utilizar como punto de corte para realizar el diagnóstico de EC sin biopsia una cifra de 42,5 veces el límite superior de la normalidad (38).
El CC debe realizarse en aquellos grupos definidos como de riesgo con alta probabilidad de EC (1–4,8,10) (tabla 6). En los familiares de segundo grado de pacientes con EC está también incrementada la prevalencia, como puede verse en las tablas 3, 4 y 5, sin embargo, no se considera indicado el cribado en estos casos salvo que existan dos o más familiares de segundo grado afectados (47). En los casos de déficit de IgA deben utilizarse anticuerpos tipo IgG anti péptidos deaminados (DGP-IgG). Estos anticuerpos tienen una sensibilidad de 84,4%, una especificidad de 98,2%, un valor VPP de 98,2% y un VPN de 86,8%; dan lugar a un mayor número de falsos positivos, por lo que su uso debe limitarse a estos casos. Otra indicación para el uso de los DGP-IgG son los menores de 2 años, ya que son precisamente este tipo de anticuerpos los primeros en aparecer cronológicamente. Unos niveles de DGP-IgG superiores a 10 U tiene una sensibilidad de 71,4% y una especificidad de 82,2% (1–3,25–27,34).
Un colectivo de particular importancia son las mujeres embarazadas con EC no diagnosticada, ya que los resultados obstétricos son peores en ellas. Los estudios de Arvanitakis y Saccone (39,40) muestran que hay una mayor frecuencia de abortos, con un riesgo relativo (RR) de 1,35 (IC 95%: 1,1-1,65), retraso de crecimiento intrauterino con RR: 1,68 (IC95%: 1,34-2,1), mortinatos RR: 1,57 (IC 95%: (1,17-2,1), recién nacidos pretérmino RR: 1,29 (IC 95%: 1,12-1,49) y parto por cesárea RR: 1,1 (IC 95%: 1,02-1,16). Resultados estadísticamente significativos frente a las gestantes sin EC.
Se estima que existe un incremento de mortalidad por todas las causas en la EC. Este aumento de mortalidad puede medirse mediante la tasa estandarizada de mortalidad (SMRI) que, en la EC, SMRI= 2 (IC 95%: 1,5-2,7%). Una elevada proporción de este incremento de mortalidad es atribuible a cáncer y va ligado a los pacientes mayores de 40 años, sintomáticos, graves, no a los asintomáticos o paucisintomáticos con anticuerpos positivos. Si nos referimos sólo a los EC que tienen neoplasias el SMRI es de 1,61 (IC95%: 1,19-2,13) (41).
En un amplio estudio de cohortes realizado en Suecia sobre 11 109 personas con EC, la tasa estandarizada de incidencia (SIR) de linfoma no Hogdkin es 6,6 veces más alta en la población con EC (IC 95%: 5-8.6) (41).
Determinación del Antígeno del sistema HLA:
Hay dos genes que codifican las moléculas HLA-DQ2, son los denominados DQA1*05 y DQB1*02. La molécula del antígeno HLA-DQ2 se une en la lámina propia intestinal a los péptidos de la gliadina transformados por la transglutaminasa tisular y los presenta a los linfocitos CD4+, iniciándose entonces la respuesta inflamatoria perjudicial para la mucosa intestinal (22,24–27,43–49). En nuestro medio la molécula HLA´DQ2 (DQA1*05 y DQB1*02) la expresan el 97% de los pacientes con EC, mientras que en la población control sólo se presenta en el 36,5%. Esto significa que esta prueba tiene un elevado VPN para descartar pacientes que no son susceptibles de presentar EC. Esto permite no reiterar el CC en pacientes de riesgo que no tengan este marcador. Los HLA no sirven por sí solos para el cribado de EC por su bajo VPP (43-49). Los HLA sirven en cambio para descartar la EC en familiares de EC, grupos de riesgo y búsqueda de casos (BC) (figura 2).
Búsqueda de casos (“Case finding”) de EC:(25,43-49)
La BC es un término de significado muy parecido al de cribado en población de riesgo. Se trata de buscar activamente casos no diagnosticados de EC en grupos que, o bien tienen un riesgo más alto (tabla 6) o que presentan alguno de los síntomas sugestivos de EC (tabla 7). La BC debe realizarse con determinaciones combinadas de HLA y la tTGA. En el caso de disponer de micrométodos, como el POC test de punción digital, debe realizarse en primer lugar la determinación de los HLA y en el caso de que estos resulten negativos proceder con la tTGA. El colectivo de HLA no DQ2/DQ8 debe excluirse de cribados ulteriores debido a su alto VPN.
Debe, no obstante, mantenerse un alto nivel de sospecha y realizar los test oportunos en caso de presentarse en la clínica síntomas sospechosos de EC. En España y a fecha de abril de 2025 muchos centros de atención primaria no disponen de estos micrométodos que permitirían una gestión más rápida y eficiente del proceso diagnóstico de EC.
Existen dos métodos de BC, la forma activa en la que es el paciente quien tiene la iniciativa de informar al médico de los síntomas que padece. En la forma pasiva de BC corresponde al médico preguntar sistemáticamente al paciente si presenta algunos de los síntomas de la tabla 7. Algunos investigadores, como es el caso del grupo de Catassi (2), defienden que la estrategia de BC no es válida ya que se necesitaría realizar la BC sobre más de un 50% de la población. Catassi y Lionetti (2,7) aportan los datos de un estudio italiano, SIGENP, sobre CC en el que se muestra que los síntomas sugestivos de EC fueron comunes entre la población de control y que el porcentaje de pacientes con EC detectados con la estrategia de case finding fue del 40%. La mayoría de los casos de EC quedaron sin detectar con la BC. A pesar de todo la mayoría de los grupos de expertos y agencias recomiendan hoy en día la BC como estrategia más razonable (20,22,24,25,43-53) (ver tabla 9). Se han desarrollado modelos de predicción de la EC con los principales factores de riesgo como es la edad, el sexo, tener familiares de primer grado de EC y HLA. Con estos datos existen algoritmos que describen la probabilidad de desarrollar EC a lo largo del tiempo y con qué intervalos de tiempo realizar CC (24,42,51), como puede verse en el siguiente enlace: https://hputter.shinyapps.io/preventcd/ (53).
El CC cumple con muchos de los criterios de Younger and Wilson (54) (tabla 8) para introducirlo como programa de salud pública a realizar en la población general, siendo además coste efectivo; sin embargo, hay autores que opinan que hay mucha incertidumbre sobre cuál sería la repercusión del diagnóstico en la vida de las personas con EC asintomática o paucisintomática y su grado de adherencia a la DSG. Tampoco existe consenso sobre cuál sería el programa de cribados a lo largo de la vida ya que con un sólo cribado no se detectarían todos los casos (50,51).
Es de destacar que el parlamento italiano ha promulgado en 2023 una ley para el cribado universal de diabetes tipo1 y EC durante la infancia (55) (ver tabla 9).
Tabla 6. Situaciones de riesgo de enfermedad celíaca.
- Familiares de 1º de EC*
- Enfermedades autoinmunes en la familia
- Sd. de Down
- Sd. de Turner
- Sd. de Williams
- Diabetes tipo 1
- Genética HLA DQ2/DQ8**
|
* En familiares de 2º si hay más de un familiar con EC
**https://hputter.shinyapps.io/preventcd/
Tabla 7. Síntomas para realizar la búsqueda de casos
- Dolor abdominal crónico
- Diarrea de larga duración
- Distensión abdominal
- Estreñimiento crónico
- Reflujo gastroesofágico
- Vómitos recurrentes
- Anemia crónica
- Pérdida de peso
- Alteraciones del esmalte
- Aftas de repetición
- Irritabilidad de larga duración
|
En la figura 2 se puede ver representada la forma de realizar en CC secuencial HLA y T-TGA.
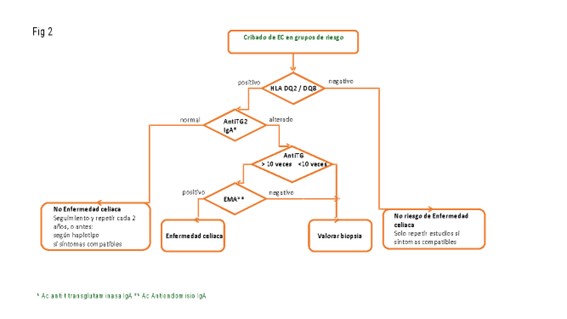
Pregunta 3.- ¿Cuáles son los daños potenciales derivados del cribado de la EC?
El CC puede producir daños potenciales a través de un fenómeno de etiquetado. Recibir el diagnóstico de EC supone modificar hábitos derivados de la dieta sin gluten (DSG), producir miedo o hipervigilancia sobre la composición de la dieta. Las comidas fuera de casa imponen limitaciones en actividades sociales, escolares o laborales. En un estudio español realizado en Madrid con menores con EC, la calidad de vida relacionada con la salud (CVRS) fue mejor en los menores de 2 años, tiempo de diagnóstico de EC superior a 8 años, formas clásicas de enfermedad y cumplidores de la DSG y peor en los que tenían dificultades sociales. No se produjeron sin embargo diferencias por edad o sexo (56).
Otras investigaciones informan de limitaciones en la vida diaria de los menores con EC en aspectos como hablar de la EC, actividades, comer fuera de casa, campamentos escolares, etc. Otros trabajos afirman que la CVRS no se ve deteriorada por el seguimiento de una DSG.
Existe una amplia bibliografía sobre cómo influye la EC sobre la CVRS, tanto en adultos como en niños (55–66) y cómo con cierta frecuencia se producen trastornos de salud mental, ansiedad, depresión, trastorno obsesivo respecto a la comida, fobias sociales, trastornos de la conducta alimentaria y otros (56–68). Esta cuestión se analizará más detalladamente en la pregunta 4.
Pregunta 4.- ¿Cuáles son los daños potenciales de la detección precoz de EC?
La DSG de por vida es el único tratamiento posible y capaz de mejorar los síntomas y las complicaciones a largo plazo (1–4,24). Hay autores que informan de un menor número de síntomas y de mejor CVRS en pacientes con EC tras un período de un año de DSG (61). En el estudio de Torres (56), se informa de una mejor CVRS en los casos de EC diagnosticados antes de los 2 años de vida y en los de más prolongado tiempo de seguimiento. Se vieron peores resultados en los no adherentes a la DSG, en familias con dificultades económicas y en las formas clásicas de presentación de la EC. Otros autores sin embargo no han comprobado estos resultados (1–4). El estudio de Coburn de 2019 (68) es una revisión sistemática que analiza la presencia de comorbilidad psiquiátrica en adolescentes con EC. Examina 26 publicaciones, entre ellas 9 estudios observacionales, uno de caso control y un ensayo clínico. De todos ellos hay que destacar el estudio de Butwica, que encuentra una probabilidad 1,4 veces mayor de comorbilidad psiquiátrica, incluyendo trastorno del estado de ánimo, ansiedad, depresión, trastornos de conducta alimentaria y trastorno del espectro autista (TEA). En el estudio italiano de Calderoni se muestra cómo los TEA tienen una prevalencia de un 2,6% entre los afectados de EC, una cifra mucho más elevada que la población italiana de referencia (p=0,0246). Es llamativo el estudio Pynönnen, en el que el riesgo de depresión a lo largo de la vida es de 31% vs 7%, OR: 6,06 (IC 95%: 1,18-31,3; P<0,04). Las conductas disruptivas y el trastorno por déficit de atención con hiperactividad fueron también más frecuentes: 28% vs 3%, OR: 10,67 (IC 95%: 1,24-92; p<0,04). La misma revisión recoge los datos del estudio de Sevinc en Turquía en 2017. Se trata de un estudio de casos y controles con 52 individuos con EC vs 40 controles sanos y señala que la calidad de vida relacionada con la salud obtuvo peores puntuaciones en todas las áreas. El estudio de Wagner de 2015, realizado en adolescentes entre 10-20 años muestra que los diagnosticados tardíamente de EC presentan peores puntuaciones en CVRS comparado con los de diagnóstico temprano, X2: 7,6 p: 0,022. Estos últimos tuvieron además problemas de relación con sus pares respecto de los controles (X2: 7,44 p: 0,024), peores puntuaciones en CVRS y peor todavía en los nos seguidores de la DSG, anticipando con un mayor probabilidad problemas futuros de salud (X2: 14,8 p: 0,003) y un malestar mayor (X2: 7,94 p: 0,047). Los adolescentes con diagnóstico tardío mostraron una mayor carga relacionada con la EC (X2: 15,63 p<0,0001) (68) siendo X2 el estadístico que expresa la diferencia entre los valores observados y los esperados.
Analizaremos también las tres revisiones sistemáticas realizadas entre 2020 y 2022 sobre EC, calidad de vida y bienestar psicosocial. La revisión de Ho (65) analiza 43 artículos evaluando cuatro aspectos como son bienestar social, adaptación psicológica, salud mental y función social. Hasta un 68,8% de los niños muestran angustia relacionada con EC y entre ellos, un 27% tiene vergüenza de hablar de su EC fuera de casa. El 50% sienten que su EC es una carga para otros. El 46% de los adolescentes tienen vergüenza de comer DSG. Al 30% de los niños y al 48,3% de adolescentes les humilla su EC. Entre los adolescentes hasta a un 60% no les gusta llevar comida sin gluten a fiestas y cumpleaños. En el funcionamiento social, hasta 77% se sienten diferentes debido a la EC. Hasta el 56% se sienten incomprendidos por profesores y amigos. Se sienten marginados en casa o en el colegio hasta un 51,1%. Hasta un 33% piensan que no les invitan a fiestas debido a su EC. El estudio de Nikniaz (59) analiza 26 estudios con un número de 2774 en los que se evalúa la CVRS usando diferentes cuestionarios como HRQL, PedsQL, AUQUEI y la adherencia a la dieta sin gluten, generalmente evaluada con el cuestionario CDDUX. En este estudio no se encuentran diferencias entre CVRS entre sanos y personas con EC, sin embargo hay diferencias en subgrupos y se piensa que puede depender de los cuestionarios utilizados. Es interesante destacar que informan de una peor puntuación CVRS informada por los padres. En cualquier caso, hay una amplia bibliografía sobre el impacto de la DSG sobre la CVRS (56-68).
Pregunta 5.- ¿Cuáles son los daños derivados de la dieta sin gluten (DSG)?
La DSG plantea una serie de carencias nutricionales que, de no ser compensadas, pueden conducir a deficiencias nutricionales como por ejemplo déficit de micronutrientes como Fe, Zn, fibra (69–74). La DSG da lugar a un consumo más elevado de grasas saturadas, contribuye a la obesidad y a problemas cardiovasculares en adultos, osteopenia, desequilibrio en el microbiota intestinal. Estos desequilibrios pueden darse incluso en pacientes cuya mucosa intestinal está en fase de recuperación (74). También se citan deficiencias en vitamina B6, B12, D y folato, así como elevaciones de la homocisteína. Otros trabajos no han informado de diferencias nutricionales significativas tanto en pacientes con EC como tampoco en la asociación con diabetes mellitus. En el metaanálisis realizado por Xin en 2022 se pudo apreciar cómo entre pacientes con y sin DSG no hubo diferencias en parámetros como peso, talla, IMC, circunferencia abdominal, pero sí la hubo en el subgrupo de EC con mayores incrementos en peso e IMC en pacientes con EC y por tanto con mayor riesgo de obesidad (73).
En el estudio narrativo realizado por Di Nardo (71) que revisa 35 artículos, se describen las deficiencias nutricionales encontradas en niños con EC y se afirma que estas ocurren en el 20-38% de los casos de niños. En primer lugar, el consumo de grasas saturadas es mayor que en los no celíacos, aunque ambos grupos están por encima de las recomendaciones y en ambos se da un desequilibrio en la proporción entre grasas saturadas versus poliinsaturadas. El consumo de fibra es también menor en la EC. Los carbohidratos consumidos en los pacientes con EC tienen un índice glicémico mayor al ser el gluten un inhibidor de la hidrólisis de los almidones. Se da también un déficit de Fe, Cu, Zn, Folatos, Vitaminas A, D, B6, B12, incluso en pacientes aparentemente bien nutridos. El déficit de vitaminas del grupo implica un aumento de la homocisteína que es un factor independiente para el riesgo cardiovascular. El déficit de Zn implica retraso de crecimiento, los de Cu y Vit D alteraciones en la inmunidad y osteopenia. Todas estas deficiencias pueden influir en los síntomas extraintestinales de la EC como ataxia, demencia, neuropatía, epilepsia (69).
Pregunta. 6.- ¿Cuáles son los costes del Cribado de la EC y de la DSG?
Respecto a los estudios económicos es relevante el estudio de Nörstrom (75,76) a partir del estudio nacional sueco ETICS de coste-efectividad mediante un análisis según el método de Markov. Encuentran resultados favorables.
Herscovici realiza asimismo un estudio markoviano de coste-efectividad que encuentra favorable al cribado si se dan estas circunstancias: ratio estandarizada de mortalidad entre cribados y no cribados superior a 1,5, prevalencia mayor de 0,87%, grado elevado de adherencia y lapso entre inicio de síntomas y diagnóstico superior a 5,9 años (77).
El National Institute For Health Care and Research y el Health Technology Assesment del Reino Unido, informan que el coste-efectividad del cribado mediante serología a toda la población, asumiendo una prevalencia del 1%, es de 20 000 libras por año ajustado ganado en buena calidad de vida (QUALY). El beneficio neto del Incremental Cost-Efectiveness Ratio (ICER) es de 5080-6493 libras para cada hombre y de 4829 libras para cada mujer. El beneficio neto es similar realizando serología tTGA EMA-IgA o doble tTGA con HLA (24).
Suasnabar en 2024 (78) estudia el coste-efectividad tanto para el CC como para la BC mediante un método también markoviano y el resultado es también favorable tanto para el cribado como para la detección oportunista.
Long analiza los costes médicos de la EC con los registros de pacientes con EC del condado de Olmstead. Este autor encuentra una diferencia de 466$ respecto de los costes médicos de los mismos pacientes un año antes del diagnóstico. Cuando comparan los costes médicos (79) acumulados durante un período de 4 años la diferencia promedio respecto de sus controles sin EC es de unos 4000$.
Soler realiza en Suiza (80) un estudio en el que pregunta a la población la suma que estarían dispuestos a pagar al año por verse libres de la EC, resultando en unos 1000 € anuales esta cantidad.
Respecto al coste de la cesta de la compra, los productos elaborados sin gluten son menos accesibles y mucho más caros que a sus homólogos con gluten, esta variación se da entre países, regiones e incluso entre mercados de diferentes zonas de una ciudad, lo que conduce a una carga económica y representa un gasto que sólo es menor que en enfermedades como la insuficiencia renal crónica, diabetes, insuficiencia cardíaca congestiva, hipertensión (81). En estudios realizados en España sobre productos de la cesta de la compra básicos, se aprecia que el coste de los alimentos libres de gluten es hasta un 395% mayor que sus homólogos con gluten.
En el estudio de Lee de 2019 se informa de que los precios en EE. UU. en 2006, para productos sin gluten, fueron globalmente un 183% más altos que sus homólogos con gluten (p<0,001), aunque es cierto que la entrada de proveedores masivos de productos alimenticios para cadenas de supermercados supuso una rebaja al 139% y mejoró la disponibilidad, aunque esta varía en función de regiones, localidades o incluso diferentes calles de una ciudad (82).
En otro estudio realizado en España (83), comparando 216 marcas de productos con y sin gluten, se puede apreciar que los productos etiquetados como sin gluten tienen un coste casi seis veces mayor. En este análisis se describe cómo estos productos contienen menos proteínas, más azúcares y más grasas saturadas. Existe el problema de la disponibilidad, ya que los supermercados más económicos son los que tienen mayor escasez de estos productos.
Preguntas Clínicas Relacionadas:
Pregunta 7.- ¿Cuál es la adherencia de las personas con EC a la DSG?
Hay investigadores que afirman que la adherencia a la DSG es similar tanto en el grupo diagnosticado por cribado como en el grupo diagnosticado por síntomas clínicos. Además, el grupo de cribado tuvo mejores puntuaciones en escalas de salud mental que los de la población general y fueron comparables en otros aspectos de salud (66,84–94).
En el estudio de Mehta en el contexto del Ensayo TEDDY sobre 290 pacientes utilizando cuestionarios validados se encontró una adherencia completa del 73% a los 2 años del diagnóstico y del 67% a los 5 años, y una adherencia inconstante en el 1% a los 2 años y 15% a los 5 años (91). En España el estudio de Casellas de 2020, que realiza una encuesta nacional sobre adherencia a la DSG en pacientes con EC, encuentra un 20% de adultos con EC que no realizan ningún tipo de seguimiento de su enfermedad. Las razones dadas para este mal seguimiento eran considerar que habían sido dados de alta y tenían dificultades económicas para seguir la DSG. A pesar de todo el 93,3% de los adultos diagnosticados después de los 18 años seguían casi siempre la DSG y el 92,9% de los diagnosticados antes de los 18 años (66).
Se ha discutido si la adherencia al tratamiento difiere en pacientes con EC diagnosticada por CC o sintomatología clínica. Existen estudios que afirman que la adherencia a la DSG es similar o mejor (84-94) tanto en el grupo diagnosticado por CC, como en el grupo diagnosticado por síntomas clínicos. Además, el grupo de CC tuvo mejores puntuaciones en escalas de salud mental que los de la población general y fueron comparables en otros aspectos de salud. Analizamos los datos de la revisión sistemática realizada en 2020 por el grupo de Myleus (93) sobre adherencia a la DSG en pacientes pediátricos. Este estudio analiza 49 trabajos realizados en 24 países sobre 7850 pacientes con EC. La adherencia fue muy variable entre los diferentes trabajos, entre 23-98% con una mediana entre 75-87%. La variabilidad no se correlacionó con el cuestionario de valoración de la DSG. Hubo diferencias entre regiones: Escandinavia 90%, Europa 74%, Norteamérica 79% y otros países 77%. La adherencia fue peor en adolescentes. No hubo diferencias por sexo, tampoco por historia familiar de EC ni por el hecho de haber sido o no diagnosticado por su sintomatología. Tampoco influyó el tamaño de la población en la que vivían. No hubo diferencias por edad al diagnóstico ni tiempo de evolución de la enfermedad. Los padres con mejores conocimientos daban lugar a una mayor adherencia, así como ser socio de una asociación de EC. En el trabajo de Torres (56) indica cómo la CVRS fue peor en aquellos niños con mala adherencia o con dificultades para seguir la DSG por motivos sociales.
En el estudio TEDDY el 73% de los pacientes con EC seguían siendo adherentes de forma estricta (89) a los 2 años y 67%% a los 15 años. Fueron más adherentes los que tenían familiares de 1º grado con enfermedad celiaca y dentro del grupo de los adherentes, los europeos consumían menos gluten en los registros que los norteamericanos.
En el estudio de una cohorte italiana de adultos diagnosticados de EC mediante cribado y a los que se aplica un seguimiento de 20 años se puede observar que el 56% tienen una adherencia óptima a la DSG, un 20% abandonan la DSG y hasta en 16% aparecen otras enfermedades autoinmunes (94).
Pregunta 8.- ¿La introducción del gluten en mayor cantidad diaria o a una edad determinada influye en el desarrollo posterior de EC?
Pregunta 9.- ¿La introducción del gluten durante la lactancia materna disminuye la probabilidad de desarrollo posterior de EC?
A efectos prácticos abordaremos estas dos preguntas de forma conjunta. Partimos de la revisión sistemática realizada por el grupo de Szajewska (95–103).
En la revisión anterior publicada por el mismo grupo de autores en 2016 no se aprecia relación alguna entre LM de cualquier duración y EC. En 2024 la ESPGHAN realiza una nueva revisión sobre lactancia materna, introducción del gluten, cantidad ingerida, ritmo de introducción y riesgo de EC (101). Como resultado de esta revisión no se modifican las recomendaciones realizadas por la ESPGHAN en 2016 (100). Estos autores se plantean siete preguntas. En la primera se investiga la relación de la LM de cualquier duración y la incidencia de EC. Analizan una revisión sistemática con 7 artículos entre los que destaca el realizado en Irán con un diseño de caso control retrospectivo. Este artículo presenta importantes diferencias entre los casos y los controles y no permite sacar conclusiones válidas.
En la cuestión segunda investigan la edad en la que se introduce el gluten y su relación con la EC, en la que valoran una revisión sistemática con metaanálisis de 4 estudios que sugiere que existe asociación entre EC y una introducción más temprana. Sin embargo, esta conclusión no es apoyada por ensayos clínicos aleatorizados.
En la tercera pregunta se estudia si el ritmo y la edad en la que se introduce el gluten influye en la EC. Un ensayo clínico con distribución aleatoria sugiere una asociación entre EC e introducción a los 6 meses del gluten frente a la introducción a los 12 meses. No obstante, cuando se analiza a más largo plazo la introducción más temprana del gluten no influye en el índice acumulativo de EC después de los 3 años.
La cuarta cuestión investiga si la introducción del gluten durante el destete y posteriormente influye en la EC. En estudios de cohortes parece que una ingesta mayor comportaría más EC. En estos estudios se han visto, sin embargo, dificultades en la valoración de la ingesta, cambios de hábitos de consumo y problemas en los análisis estadísticos. Algunos de estos estudios muestran más autoinmunidad y más EC, pero no establecen un umbral de seguridad en la cantidad diaria de gluten ingerido por día.
La quinta pregunta se refiere a si el tipo de alimentos con gluten ingeridos influyen en el desarrollo de EC. En un estudio realizado en Suecia con metaanálisis de 2 estudios de caso control se sugiere una mayor incidencia de EC cuando el gluten se mezcla con fórmula frente a la mezcla con sólidos. El estudio sueco TEDDY realizado con población genéticamente predispuesta a diabetes 1 y EC, indica un mayor nivel de autoinmunidad en edades de 9, 12 y 18 meses en los consumidores de gluten frente a los que no lo son, pero no permite sacar ninguna conclusión respecto de la EC.
La sexta cuestión se refiere a si el consumo de gluten por la madre gestante influye en el posterior desarrollo de EC, no pudiendo obtener pruebas para modificar las recomendaciones actuales.
La séptima pregunta trata de si en una población genéticamente predispuesta a EC la cantidad de gluten ingerida tiene efectos diferentes según el genotipo HLA. En el estudio DAISY no se aprecia asociación entre EC o autoinmunidad a los 12 meses y cantidad de gluten ingerido. En el estudio Prevent CD (47,95) tampoco se aprecia asociación a los 5 años, excepto para los que muestran el haplotipo DQ2.2/DQ7, Hazard Ratio (HR): 5,81 (IC 95%: 1,18-28,7). En el estudio TEDDY tomando los que ingerían más de 5 grs/d de gluten y estaban en el primer tercil de consumo, hubo mayor incidencia de EC a mayor consumo, pero sin embargo no se vio ninguna asociación con los diferentes genotipos HLA, por lo que se deduce que esta asociación no tiene que ver con estos haplotipos.
Resumen de la evidencia:
- No hay pruebas de buena calidad para apoyar el cribado masivo de EC en población general sana menor de 18 años, tampoco en adultos.
- No está claro el impacto de la búsqueda de casos sobre la calidad de vida ni tampoco la estrategia para repetir el cribado en los casos negativos a lo largo de la vida.
- Hay pruebas de buena calidad para apoyar el cribado en población de riesgo, familiares de 1º de pacientes con EC, diabetes tipo 1, tiroiditis, enfermedades autoinmunes, baja talla, anemia crónica y síndromes de Down, Turner y Williams.
En la tabla 8 podemos ver los criterios de Jungner & Wilson para el CC, en la tabla 9 las recomendaciones de los principales grupos de expertos, y en la 10 y 11 las recomendaciones de PrevInfad.
Tabla 8. Criterios de Jungner & Wilson sobre cribado.
|
Debe ser un problema de salud importante
|
Sí
|
|
Debe haber un tratamiento aceptado
|
Sí
|
|
Medios de diagnóstico y tratamiento disponibles
|
Sí
|
|
Pruebas diagnósticas adecuadas
|
Sí
|
|
Pruebas aceptables para la población
|
Sí
|
|
La historia natural de la enfermedad incluyendo el desarrollo de la enfermedad latente debe ser conocido
|
Incertidumbre en formas latentes y silentes
|
|
Debe haber una política de quienes tratar como pacientes
|
Incertidumbre en formas latentes y silentes
|
|
El coste debe estar equilibrado con los gastos médicos en su conjunto
|
Sí
|
|
La búsqueda de casos debe ser parte de un programa establecido y continuado
|
Incertidumbre de cuántos cribados realizar a lo largo de la vida del paciente
|
RECOMENDACIONES DE OTROS GRUPOS DE EXPERTOS
Tabla 9. Recomendaciones de grupos de expertos
|
USPSTF
|
2017
|
No
|
Factores de riesgo (tabla 6)
BC*Listado de síntomas (tabla 7)
|
|
NICE & Celiac UK
|
2015
|
No
|
Factores de riesgo (tabla 6)
BC Listado de síntomas (tabla 7)
|
|
ESPGHAN
|
2019
|
No
|
Factores de riesgo (tabla 6)
BC Listado de síntomas (tabla 7)
|
|
NHS
|
2022
|
No
|
Factores de riesgo (tabla 6)
BC Listado de síntomas (tabla 7)
|
|
AEPap
(España)
|
2024
|
No
|
Factores de riesgo (tabla 6)
BC Listado de síntomas (tabla 7)
|
|
Glutescreen Project
(Holanda)
|
2022
|
No
|
Factores de riesgo (tabla 6)
BC Listado de síntomas (tabla 7)
|
|
American College
Gastroenterology
|
2023
|
No
|
Factores de riesgo (tabla 6)
BC Listado de síntomas (tabla 7)
|
|
Ministerio della salute i Camera dei deputati de il senato della Republica italiana (legge)
|
2023
|
Sí
|
Población gral 1-17 años cribado de EC y Diabetes 1
|
* BC: Búsqueda de casos
RECOMENDACIONES DE PREVINFAD
Tabla 10. Recomendaciones de PrevInfad
|
Cribado universal en menores de 18 años
|
Débil en contra
|
Se sugiere no hacer
|
|
Cribado en grupos de riesgo
|
Fuerte a favor
|
Se recomienda hacer
|
|
Determinaciones combinadas HLA y tTGA
|
Fuerte a favor
|
Se recomienda hacer
|
|
Si se dispone de micrométodos de punción digital, hacer primero HLA
|
Fuerte a favor
|
Se recomienda hacer
|
|
Si HLA DQ2/D8 negativos no cribados ulteriores salvo la presencia de síntomas de enfermedad celíaca
|
Fuerte en contra
|
Se recomienda no hacer
|
Tabla 11. Recomendaciones basadas en buena práctica clínica
|
Supervisar la posibilidad de peor CVRS* y problemas de salud mental en menores con EC, especialmente en adolescentes, dificultades sociales y mala adherencia a la DSG
|
|
Supervisar de forma estricta la adherencia de los menores con EC a la DSG **
|
|
Fomentar la educación de las familias de menores con EC sobre la enfermedad y DSG
|
|
No existen pruebas de buena calidad que permitan relacionar el desarrollo de EC con el amamantamiento ni con el destete ni con la cantidad de gluten ingerida.
La leche humana se reconoce como el alimento idóneo para todos los niños por sus probados beneficios en la salud de la madre y el niño. La OMS y otras organizaciones recomiendan la lactancia materna exclusiva durante los primeros seis meses y al menos hasta los dos años complementada con otros alimentos
https://previnfad.aepap.org/recomendacion/lactanciamaterna-rec
|
*CVRS: Calidad de vida relacionada con la salud
** DSG: Dieta sin gluten
ESTRATEGIA DE BÚSQUEDA
1.- ("Celiac Disease/epidemiology"[Mesh] OR "Celiac Disease/organization and administration"[Mesh] OR "Celiac Disease/prevention and control"[Mesh] )) AND ("Mass Screening/adverse effects"[Mesh] OR "Mass Screening/classification"[Mesh] OR "Mass Screening/diagnosis"[Mesh] OR "Mass Screening/economics"[Mesh] OR "Mass Screening/epidemiology"[Mesh] OR "Mass Screening/ethics"[Mesh] OR "Mass Screening/standards"[Mesh] )
2.- ("Celiac Disease"[Mesh]) AND "Mass Screening"[Maj Filters: Clinical Trial, Meta-Analysis, Randomized Controlled Trial, Review, Systematic Review, in the last 10 years – PubMed.”
3.- "Glutens"[Mesh] AND "Celiac Disease"[Mesh] AND ("2008/09/01"[PDat] : "2013/08/30"[PDat] AND "infant"[MeSH Terms]
4.- ("Celiac Disease/diagnosis"[Majr:NoExp]) AND "Reagent Kits, Diagnostic"[Majr:NoExp]
5.- ("Celiac Disease"[Mesh]) AND "Prevalence"[Mesh]
6.- "Breast Feeding"[Mesh] AND ("Celiac Disease/diet therapy"[Mesh] OR "Celiac"[Mesh])
7.- ("Breast Feeding"[Mesh]) AND "Celiac Disease"[Maj Filters: Clinical Trial, Meta-Analysis, Randomized Controlled Trial, Systematic Review, in the last 10 years – PubMed
8.- ("Diet, Gluten-Free/adverse effects"[Mesh] OR "Diet, GlutenFree/psychology"[Mesh] OR "Diet, Gluten-Free/standards"[Mesh] OR "Diet, Gluten-Free/trends"[Mesh]) Filters: Clinical Trial, Meta-Analysis, Randomized Controlled Trial, Systematic Review, in the last 5 years
9.- "economics" [Subheading]) AND "Celiac Disease"
10.- (("Celiac Disease"[Mesh]) AND "Patient Compliance – PubMed
11.- ("Celiac Disease"[Mesh]) AND (“Quality-Adjusted Filters: Clinical Trial, MetaAnalysis, Randomized Controlled Trial, Systematic Review, in the last 5 years
12.- ("Treatment Adherence and Compliance"[Mesh]) AND ("Diet, GlutenFree/psychology"[Majr] OR "Diet, Gluten-Free/trends"[Majr])
13.- (("Celiac Disease"[Mesh]) AND "Diet, Gluten-Free/economics"[Majr:NoExp]) AND ("Costs and Cost Analysis"[Mesh] OR "Economics"[Mesh] OR "economics" [Subheading] OR "Cost of Illness"[Mesh] OR "Cost Sharing"[Mesh])
14.- HLA typing and 'celiac disease' and 'mass screening' (("Celiac Disease"[Majr]) AND "Histocompatibility Testing"[Majr]) AND "Mass Screening"[Majr]
15.- AND (2020:py OR 2021:py OR 2022:py OR 2023:py OR 2024:py) AND ('case finding'/de OR 'meta analysis'/de OR 'practice guideline'/de OR 'systematic review'/de)
16.- AND (2020:py OR 2021:py OR 2022:py OR 2023:py OR 2024:py) AND ('meta analysis'/de OR 'systematic review'/de)
Buscadores: Pubmed, Embase, Guía Salud, National Guidelines Clearinghouse, Tripdatabase, Fisterrae, Cochrane Library, Clinical Trials Gov, Health Technology Assesment Database, NHS Economic Evaluation Database, Pediatria basada en la evidencia, Preevid, Perlas Cochrane. Trip Answers 54 ("Celiac Disease"[Mesh]) AND "Diet, Gluten-Free/adverse effects.
BIBLIOGRAFÍA
- Caio G, Volta U, Sapone A, Leffler DA, De Giorgio R, Catassi C, et al. Celiac disease: A comprehensive current review. BMC Medicine. 2019;17(142):2-20.
- Catassi C, Verdu EF, Bai JC, Lionetti E. Coeliac disease. Lancet. 2022;399:2413–26.
- Stahl M, Liu E. Uptodate 2023 January 20. Epidemiology, Pathogenesis and clinical Manifestations of Celiac Disease in Children.
- Polanco Allué I, et al. M de S y AS. Grupo de trabajo del Protocolo para el diagnóstico precoz de la enfermedad celíaca. Protocolo para el diagnóstico precoz de la enfermedad celíaca. Ministerio de Sanidad, Servicios Sociales e Igualdad. Servicio de Evaluación del Servicio Canario de la Salud (SESCS); 2018. Disponible en: https://www.sanidad.gob.es/profesionales/prestacionesSanitarias/publica…
- Taraghikhah N, Ashtari S, Asri N, Shahbazkhani B, Al-Dulaimi D, Rostami-Nejad M, et al. An updated overview of spectrum of gluten-related disorders: Clinical and diagnostic aspects. BMC Gastroenterology. 2020;20:258.
- Fasano A. Clinical presentation of celiac disease in the pediatric population. Gastroenterology. 2005;128(4 SUPPL. 1).S68-73.
- Lionetti E, Pjetraj D, Gatti S, Catassi G, Bellantoni A, Boffardi M, et al. Prevalence and detection rate of celiac disease in Italy: Results of a SIGENP multicenter screening in school-age children. Digestive and Liver Disease. 2023;55(5):608–13.
- Gatti S, Lionetti E, Balanzoni L, Verma AK, Galeazzi T, Gesuita R, et al. Increased Prevalence of Celiac Disease in School-age Children in Italy. Clinical Gastroenterology and Hepatology. 2020;18(3):596–603.
- Gheshlagh RG, Rezaei H, Goli M, Ausili D, Dalvand S, Ghafouri H, et al. Prevalence of celiac disease in Iranian patients with type 1 diabetes: A systematic review and meta-analysis. Indian Journal of Gastroenterology. 2020;39:419–25.
- Zhou WY, Liu XY, Wang MM, Liang LP, Liu L, Zheng DK, et al. Prevalence of celiac disease in China: Meta-analysis and serological survey in high-risk populations. Vol. 22, Journal of Digestive Diseases.2021:645–55.
- Ashtari S, Najafimehr H, Pourhoseingholi MA, Rostami K, Asadzadeh-Aghdaei H, Rostami-Nejad M, et al. Prevalence of celiac disease in low and high risk population in Asia–Pacific region: a systematic review and meta-analysis. Sci Rep. 2021;11(1):2383.
- Comas E, Mariné M. Cribado poblacional para la enfermedad celíaca: ¿ya está justificado? Gastroenterología y hepatología continuada. 2008;7;86-90.
- Parra-Medina R, Molano-Gonzalez N, Rojas-Villarraga A, Agmon-Levin N, Arango MT, Shoenfeld Y, Anaya JM. Prevalence of celiac disease in Latin America: a systematic review and meta-regression. PLoS One. 2015;10(5):e0124040.
- Celdir MG, Jansson-Knodell CL, Hujoel IA, Prokop LJ, Wang Z, Murad MH, et al. Latitude and Celiac Disease Prevalence: A Meta-Analysis and Meta-Regression. Clinical Gastroenterology and Hepatology. 2022;20(6):e1231–9.
- Catassi C, Rätsch IM, Gandolfi L, Pratesi R, Fabiani E, El Asmar R, Frijia M, Bearzi I, Vizzoni L. Why is coeliac disease endemic in the people of the Sahara? Lancet. 1999;354:647–8.
- Manual de trabajo del grupo PrevInfad/PAPPS. Capítulo 4.1: Formulación de las preguntas y marco analítico. Disponible en: https://previnfad.aepap.org/manual-de-trabajo#4.1
- Sanabria AJ, Rigau D, Rotaeche R, Selva A, Marzo-Castillejo M, Alonso-Coello P. Sistema GRADE: Metodología para la realización de recomendaciones para la práctica clínica. Aten Primaria. 2015;47(1):48–55.
- Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, et al. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. Gac Sanit. 2018;32(2):167.e1-167.e10.
- Kemper AR, Krist AH, Tseng CW, Gillman MW, Mabry-Hernandez IR, Silverstein M, et al. Challenges in Developing U.S. Preventive Services Task Force Child Health Recommendations. Am J Prev Med. 2018;54(1S1):s63–9.
- Bibbins-Domingo K, Grossman DC, Curry SJ, Barry MJ, Davidson KW, Doubeni CA, et al. Screening for celiac disease: US preventive services task force recommendation statement JAMA. 2017;317(12):1252–7.
- Harris RP, Helfand M, Woolf SH, Lohr KN, Mulrow CD, Teutsch SM, et al. Current methods of the U.S. Preventive Services Task Force: A review of the process. Am J Prev Med. 2001;20(3):21–35.
- Mearin ML, Agardh D, Antunes H, Al-Toma A, Auricchio R, Castillejo G, et al. ESPGHAN Position Paper on Management and Follow-up of Children and Adolescents with Celiac Disease. J Pediatr Gastroenterol Nutr. 2022;75(3):369–86.
- Al-Toma A, Volta U, Auricchio R, Castillejo G, Sanders DS, Cellier C, et al. European Society for the Study of Coeliac Disease (ESsCD) guideline for coeliac disease and other gluten-related disorders. United European Gastroenterology J. 2019;7(5): 583–613.
- Elwenspoek MM, Thom H, Sheppard AL, Keeney E, O’Donnell R, Jackson J, et al. Defining the optimum strategy for identifying adults and children with coeliac disease: systematic review and economic modelling. Health Technol Assess. 2022;26(44):1-310.
- Meijer-Boekel C, Van Den Akker ME, Van Bodegom L, Escher J, Van Geloven N, Van Overveld F, et al. Early diagnosis of coeliac disease in the Preventive Youth Health Care Centres in the Netherlands: Study protocol of a case finding study (GLUTENSCREEN). BMJ Paediatr Open. 2021;5(1):e001152.
- Meijer C, Smit L, Van Overveld F, Van Geloven N, Mearin L. Early diagnosis of coeliac disease by case-finding at the Preventive Youth Health Care Centers in the Netherlands (GLUTENSCREEN) Preliminary results. Available from: https://www.glutenscreen.nl/wp-content/uploads/2021/06/Poster-case-find…
- Meijer CR, Schweizer JJ, Peeters A, Putter H, Mearin ML. Efficient implementation of the “non-biopsy approach” for the diagnosis of childhood celiac disease in the Netherlands: a national prospective evaluation 2010-2013. Eur J Pediatr. 2021;180(8):2485-92.
- Catassi GN, Pulvirenti A, Monachesi C, Catassi C, Lionetti E. Diagnostic accuracy of Iga anti-transglutaminase and Igg anti-deamidated gliadin for diagnosis of celiac disease in children under two years of age: A systematic review and meta-analysis. Nutrients. 2021;14(1):7.
- Pjetraj D, Pulvirenti A, Moretti M, Gatti S, Catassi GN, Catassi C, et al. Diagnostic Accuracy of IgA Anti-Transglutaminase Assessed by Chemiluminescence: A Systematic Review and Meta-Analysis. Vol. 16, Nutrients 2024;16(15):2427.
- Giersiepen K, Lelgemann M, Stuhldreher N, Ronfani L, Husby S, Koletzko S, et al. Accuracy of diagnostic antibody tests for coeliac disease in children: Summary of an evidence report. J Pediatr Gastroenterol Nutr. 2012;54(2):229–41.
- Husby S, Koletzko S, Korponay-Szabó IR, Mearin ML, Phillips A, Shamir R, et al. ESPGHAN Working Group on Coeliac Disease Diagnosis; ESPGHAN Gastroenterology Committee; European Society for Pediatric Gastroenterology, Hepatology, and Nutrition. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease. J Pediatr Gastroenterol Nutr. 2012;54(4):572.
- Baraba Dekanić K, Butorac Ahel I, Ružman L, Dolinšek J, Dolinšek J, Palčevski G. Is there a role of using a rapid finger prick antibody test in screening for celiac disease in children? Gastroenterol Res Pract. 2019:4504679.
- Pichler J, Zilbauer M, Torrente F, Heuschkel R, Phillips A, Salvestrini C. Feasibility of a finger prick-based self-testing kit in first-and second-degree relatives of children with coeliac disease. World J Gastroenterol. 2011;17(14):1840–3.
- Pepe A, Mandato C, Di Leo T, Boccia G, Lucaroni G, Franci G, et al. Celiac Disease on the Bed-Side: Embedding Case Finding and Screening in Hospitalized Children. Nutrients. 2023;15(23):4899.
- Valitutti F, Leonard MM, Kenyon V, Montuori M, Piemontese P, Francavilla R, et al. Early Antibody Dynamics in a Prospective Cohort of Children at Risk of Celiac Disease. Am J Gastroenterol. 2023;118(3):574–7.
- Bonamico M, Ferri M, Nenna R, Verrienti A, Di Mario U, Tiberti C. Tissue transglutaminase autoantibody detection in human saliva: A powerful method for celiac disease screening. J Pediatr. 2004;144(5):632–6.
- Bonamico M, Nenna R, Montuori M, Luparia RPL, Turchetti A, Mennini M, et al. First salivary screening of celiac disease by detection of anti-transglutaminase autoantibody radioimmunoassay in 5000 Italian primary schoolchildren. J Pediatr Gastroenterol Nutr. 2011;52(1):17–20.
- Garcés Cubel R, García Romero R, Ros Arnal I, González Irazabal Y, Hernández de Abajo G. ¿Son válidos los criterios ESPGHAN con el método de quimioluminiscencia? Análisis de los posibles errores en el diagnóstico. Anales de Pediatría. 2025;102(4):503742.
- Arvanitakis K, Siargkas A, Germanidis G, Dagklis T, Tsakiridis I. Adverse pregnancy outcomes in women with celiac disease: a systematic review and meta-analysis. Ann Gastroenterol. 2023;36(1):12–24.
- Saccone G, Berghella V, Sarno L, Maruotti GM, Cetin I, Greco L, et al. Celiac disease and obstetric complications: A systematic review and metaanalysis. Am J Obstet Gynecol. 2016;214: 225–34.
- Pelizzaro F, Marsilio I, Fassan M, Piazza F, Barberio B, D'Odorico A, Savarino EV, Farinati F, Zingone F. The Risk of Malignancies in Celiac Disease-A Literature Review. Cancers (Basel). 2021;13(21):5288.
- Swigonski NL, Kuhlenschmidt HL, Bull MJ, Corkins MR, Downs SM. Screening for celiac disease in asymptomatic children with Down syndrome: Cost-effectiveness of preventing lymphoma. Pediatrics. 2006;118(2):594–602.
- Crehuá-Gaudiza E, Barrés Fernández A, Jovaní Casano C, Latorre Tejerina M, Largo Blanco EM, Moreno Ruiz MA, et al. Diagnosis of celiac disease in clinical practice: present and future. An Pediatr (Engl Ed). 2021;94(4):223–9.
- Meijer CR, Auricchio R, Putter H, Castillejo G, Crespo P, Gyimesi J, et al. Prediction Models for Celiac Disease Development in Children From High-Risk Families: Data From the PreventCD Cohort. Gastroenterology. 2022 ;163(2):426–36.
- Paavola S, Kurppa K, Huhtala H, Saavalainen P, Lindfors K, Kaukinen K. Coeliac disease re-screening among once seronegative at-risk relatives: A long-term follow-up study. United European Gastroenterol J. 2022;10(6):585–93.
- Schesquini-Roriz KRP, Rodríguez GMF, Castellanos JCB, Martinez-Martinez L, Guerrero SB, Rodrigo C, et al. Celiac disease diagnosis: transglutaminase, duodenal biopsy and genetic tests correlations. Front Pediatr. 2024;12:1330511.
- Almazán Fernández de Bobadilla MV, Moreno Ruiz MA, Espín Jaime B. Guía de Algoritmos en Pediatría de Atención Primaria. Enfermedad Celiaca. Cribado, Diagnóstico y Seguimiento. AEPap. 2024 (en línea) consultado el 20/04/2025. Disponible en algoritmos.aepap.org
- Martínez-Ojinaga E, Fernández-Prieto M, Molina M, Polanco I, Urcelay E, Núñez C. Influence of HLA on clinical and analytical features of pediatric celiac disease. BMC Gastroenterol. 2019;19(1):91.
- Crespo Escobar P, Castillejo G, Martínez-Ojinaga E, Donat E, Polanco I, Mearin ML, et al. Ten years of follow-up of the Spanish cohort of the European PreventCD study: the lessons learned. Rev Esp Enferm Dig. 2018;110(8):493–9.
- Rubio-Tapia A, Greer KB, Limketkai B, Hill ID, Semrad C, Kelly CP, et al. Response to Catassi et al. Am J Gastroenterol. 2023;118(9):1703.
- Rubio-Tapia A, Hill ID, Semrad C, Kelly CP, Lebwohl B. American College of Gastroenterology Guidelines Update: Diagnosis and Management of Celiac Disease. Am J Gastroenterol. 2023;118(1):59–76.
- ESPGHAN 55th Annual Meeting Abstracts. J Pediatr Gastroenterol Nutr. 2023;76(S1):1–1407.
- Lebwohl B, Greco L. Can We Predict the Onset of Celiac Disease? Gastroenterology. 2022;163(2):368–9.
- Ramírez Fernández R. Documento marco sobre cribado poblacional. Ponencia de Cribado poblacional de la comisión de salud pública. Ministerio de Sanidad y Política Social. 2010; Disponible en: https://www.sanidad.gob.es/areas/promocionPrevencion/cribado/documentos…
- Legge Camera dei deputati ed il Senato della Repubblica 130/2023 Disposizione concernenti la definizione di un programma diagnostico per l’individuazioni del diabete di tipo 1 e della celiachia [Internet]. GU 2300140 Italia; Sep 27, 2023. Disponible en: https:/www.normativa.it/uri-res/N2Ls?urnr:nins:stato:legge;2023;130;130
- Torres JB, Roman E, Cilleruelo M, Marquez M, Mearin ML, Fernandez C. Health-related quality of life in Spanish children with coeliac disease. J Pediatr Gastroenterol Nutr. 2016;62(4):603–8.
- Meyer S, Rosenblum S. Activities, participation and quality of life concepts in children and adolescents with celiac disease: A scoping review. Nutrients. 2017;9(9):929.
- Möller SP, Hayes B, Wilding H, Apputhurai P, Tye-Din JA, Knowles SR. Systematic review: Exploration of the impact of psychosocial factors on quality of life in adults living with coeliac disease. J Psychosom Res. 2021;147:110537.
- Nikniaz Z, Abbasalizad Farhangi M, Nikniaz L. Systematic Review With Meta-analysis of the Health-related Quality of Life in Children With Celiac Disease. J Pediatr Gastroenterol Nutr. 2020;70(4):468–77.
- Marsilio I, Canova C, D’odorico A, Ghisa M, Zingone L, Lorenzon G, et al. Quality-of-life evaluation in Coeliac patients on a gluten-free diet. Nutrients. 2020;12(10):1–10.
- Mozzillo E, Franceschi R, Di Candia F, Francesco R, Leonardi L, Fedi L, et al. The impact of gluten-free diet on growth, metabolic control and quality of life in youth with type 1 diabetes and celiac disease: A systematic review. Diabetes Res Clin Pract. 2022;191:110032.
- Nordyke K, Norström F, Lindholm L, Stenlund H, Rosén A, Ivarsson A. Health-related quality of life in adolescents with screening-detected celiac disease, before and one year after diagnosis and initiation of gluten-free diet, a prospective nested case-referent study. BMC Public Health. 2013;13(1):142.
- Cadenhead JW, Wolf RL, Lebwohl B, Lee AR, Zybert P, Reilly NR, et al. Diminished quality of life among adolescents with coeliac disease using maladaptive eating behaviours to manage a gluten-free diet: a cross-sectional, mixed-methods study. J Hum Nutr Diet. 2019;32(3):311–20.
- Majsiak E, Choina M, Golicki D, Gray AM, Cukrowska B. The impact of symptoms on quality of life before and after diagnosis of coeliac disease: the results from a Polish population survey and comparison with the results from the United Kingdom. BMC Gastroenterol. 2021;21(1):99
- Ho WHJ, Atkinson EL, David AL. Examining the Psychosocial Well-Being of Children and Adolescents with Coeliac Disease: A Systematic Review. J Pediatr Gastroenterol Nutr. 2023;76(1):e1–14.
- Casellas F, Rodrigo L, Molina-Infante J, Vivas S, Lucendo AJ, Rosinach M, et al. Adaptación transcultural y validación del “Celiac Disease Quality of Life (CD-QOL) survey”, un cuestionario específico de medida de la calidad de vida en pacientes con enfermedad celiaca. Rev Esp Enferm Dig. 2013;105(10):585-93.
- Simsek S, Baysoy G, Gencoglan S, Uluca U. Effects of gluten-free diet on quality of life and depression in children with celiac disease. J Pediatr Gastroenterol Nutr. 2015;61(3):303–6.
- Coburn SS, Puppa EL, Blanchard S. Psychological comorbidities in childhood celiac disease: A systematic review. J Pediatr Gastroenterol Nutr. 2019;69(2):e 25–33.
- Cardo A, Churruca I, Lasa A, Navarro V, Vázquez-Polo M, Perez-Junkera G, et al. Nutritional imbalances in adult celiac patients following a gluten-free diet. Nutrients. 2021;13(8):2877.
- Barone M, Iannone A, Cristofori F, Dargenio VN, Indrio F, Verduci E, et al. Risk of obesity during a gluten-free diet in pediatric and adult patients with celiac disease: a systematic review with meta-analysis. Nutr Rev. 2023 ;81(3):252–66.
- Di Nardo G, Villa MP, Conti L, Ranucci G, Pacchiarotti C, Principessa L, et al. Nutritional deficiencies in children with celiac disease resulting from a gluten-free diet: a systematic review. Nutrients. 2019;11(7):1588.
- Crawley C, Savino N, Halby C, Sander SD, Andersen AMN, Arumugam M, et al. The effect of gluten in adolescents and young adults with gastrointestinal symptoms: a blinded randomised cross-over trial. Aliment Pharmacol Ther. 2022;55(9):1116–27.
- Staudacher HM, Gibson PR. How healthy is a gluten-free diet? Br J Nutr. 2015;114(10):1539–41.
- Xin C, Imanifard R, Jarahzadeh M, Rohani P, Velu P, Sohouli MH. Impact of Gluten-free Diet on Anthropometric Indicators in Individuals With and Without Celiac Disease: A Systematic Review and Meta-analysis. Clin Ther. 2023;45(12):e243–51.
- Norström F, Myléus A, Nordyke K, Carlsson A, Högberg L, Sandström O, et al. Is mass screening for coeliac disease a wise use of resources? A health economic evaluation. BMC Gastroenterol. 2021;21(1):159.
- Shamir R, Hernell O, Leshno M. Cost-effectiveness analysis of screening for celiac disease in the adult population. Med Decis Making. 2006;26(3):282–93.
- Hershcovici T, Leshno M, Goldin E, Shamir R, Israeli E. Cost effectiveness of mass screening for coeliac disease is determined by time-delay to diagnosis and quality of life on a gluten-free diet. Aliment Pharmacol Ther. 2010;31(8):901–10.
- Heijdra Suasnabar J, Meijer CR, Smit L, van Overveld F, Thom H, Keeney E, et al. Long-Term Cost-Effectiveness of Case Finding and Mass Screening for Celiac Disease in Children. Gastroenterology. 2024;167(6):1129-40.
- Long KH, Rubio-Tapia A, Wagie AE, Melton LJ, Lahr BD, van Dyke CT, et al. The economics of coeliac disease: A population-based study. Aliment Pharmacol Ther. 2010;32(2):261–9.
- Soler L, Borzykowski N. The costs of celiac disease: a contingent valuation in Switzerland. Eur J Health Econ. 2021;22(9):1487–505.
- Kurien M, Sleet S, Sanders DS, Cave J. Should gluten-free foods be available on prescription? BMJ (Online). 2017;356:i6810.
- Lee AR, Wolf RL, Lebwohl B, Ciaccio EJ, Green PHR. Persistent economic burden of the Gluten free diet. Nutrients. 2019;11(2):399.
- Babio N, Lladó-Bellette N, Besora-Moreno M, Castillejo G, Guillén N, Martínez-Cerezo F, et al. A comparison of the nutritional profile and price of gluten-free products and their gluten-containing counterparts available in the spanish market. Nutr Hosp. 2020;37(4):814–22.
- Webb C, Myléus A, Norström F, Hammarroth S, Högberg L, Lagerqvist C, et al. High adherence to a gluten-free diet in adolescents with screening-detected celiac disease. J Pediatr Gastroenterol Nutr. 2015;60(1):54–9.
- Sandström O, Norström F, Carlsson A, Högberg L, Van Der Palz M, Stenhammar L, et al. Five-year follow-up of new cases after a coeliac disease mass screening. Arch Dis Child. 2022;107(6):596–600.
- Al Hayek AA, Al Zahrani WM, AlAblani HM, Al Dawish MA. Metabolic control, adherence to the gluten-free diet and quality of life among patients with type 1 diabetes and celiac disease. Diabetol Metab Syndr. 2023;15(1):189.
- Mager DR, Marcon M, Brill H, Liu A, Radmanovich K, Mileski H, et al. Adherence to the Gluten-free Diet and Health-related Quality of Life in an Ethnically Diverse Pediatric Population with Celiac Disease. J Pediatr Gastroenterol Nutr. 2018;66(6):941–8.
- Hall NJ, Rubin G, Charnock A. Systematic review: Adherence to a gluten-free diet in adult patients with coeliac disease. Aliment Pharmacol Ther. 2009:30(4):315–30.
- Abu-Janb N, Jaana M. Facilitators and barriers to adherence to gluten-free diet among adults with celiac disease: a systematic review. J Hum Nutr Diet. 2020;33(6):786-810.
- Burger JPW, de Brouwer B, IntHout J, Wahab PJ, Tummers M, Drenth JPH. Systematic review with meta-analysis: Dietary adherence influences normalization of health-related quality of life in coeliac disease. Clin Nutr. 2017;36(2):399–406.
- Mehta P, Li Q, Stahl M, Uusitalo U, Lindfors K, Butterworth MD, et al. Gluten-free diet adherence in children with screening-detected celiac disease using a prospective birth cohort study. PLoS One. 2023;18(2):e0275123.
- Fueyo Díaz R, Santos SG, Asensio Martínez Á, Antonia M, Calavera S, Magallón Botaya R, et al. Adaptación transcultural y validación del Celiac Dietary Adherence Test. Un cuestionario sencillo para determinar la adherencia a la dieta sin gluten. Rev Esp Enferm Dig. 2016;108(3):138-44.
- Myléus A, Reilly NR, Green PHR. Rate, Risk Factors, and Outcomes of Nonadherence in Pediatric Patients With Celiac Disease: A Systematic Review. Clin Gastroenterol Hepatol. 2020;18 (3):562-73.
- Cozzi G, Gabbana E, Zanchi C, Giudici F, de Leo L, Ziberna F, et al. 20-Year Follow-up Study of Celiac Patients Identified in a Mass School Screening: Compliance to Gluten-Free Diet and Autoimmunity. J Pediatr Gastroenterol Nutr. 2022;74(1):91–5.
- Chmielewska A, Pieścik-Lech M, Szajewska H, Shamir R. Primary Prevention of Celiac Disease: Environmental Factors with a Focus on Early Nutrition. Ann Nutr Metab. 2015;67(supl 2):43-50.
- Szajewska H, Chmielewska A, Pieścik-Lech M, Ivarsson A, Kolacek S, Koletzko S, et al. Systematic review: Early infant feeding and the prevention of coeliac disease. Aliment Pharmacol Ther. 2012;36(7):607–18.
- Hogen Esch CE, Rosén A, Auricchio R, Romanos J, Chmielewska A, Putter H, et al. The PreventCD Study design: Towards new strategies for the prevention of coeliac disease. Eur J Gastroenterol Hepatol. 2010;22(12):1424–30.
- Agostoni C, Decsi T, Fewtrell M, Goulet O, Kolacek S, Koletzko B, et al. Complementary feeding: A commentary by the ESPGHAN Committee on Nutrition. J Pediatr Gastroenterol Nutr. 2008;46(1):99-110.
- Vriezinga SL, Auricchio R, Bravi E, Castillejo G, Chmielewska A, Crespo Escobar P, et al. Randomized Feeding Intervention in Infants at High Risk for Celiac Disease. N Engl J Med. 2014;371(14):1304–15.
- Agostoni C, Decsi T, Fewtrell M, Goulet O, Kolacek S, Koletzko B, et al; ESPGHAN Committee on Nutrition: Complementary feeding: a commentary by the ESPGHAN Committee on Nutrition. J Pediatr Gastroenterol Nutr. 2008;46(1):99-110.
- Silano M, Agostoni C, Guandalini S. Effect of the timing of gluten introduction on the development of celiac disease. World J Gastroenterol. 2010;16(16):1939-42.
- Silano M, Agostoni C, Sanz Y, et al. Infant feeding and risk of developing celiac disease: a systematic review. BMJ Open. 2016;6:e009163.
- Szajewska H, Shamir R, Auricchio R, Chmielewska A, Dolinsek J, Kivelä L, et al. Early diet and the risk of coeliac disease. An update 2024 position paper by the ESPGHAN special interest group on coeliac disease. J Pediatr Gastroenterol Nutr. 2024;79(2):438-45.