Actualizado a fecha de 9 de septiembre de 2022. Bibliografía revisada hasta mayo de 2022. El documento es completamente nuevo.
INTRODUCCIÓN
El déficit de vitamina K al nacimiento supone un factor de riesgo para desarrollar la enfermedad hemorrágica del recién nacido (EHRN). Este estado pro hemorrágico puede producir sangrados graves principalmente a nivel cutáneo, gastrointestinal y cerebral. Se puede prevenir con la administración de vitamina K en las primeras horas de vida (1).
La vitamina K interviene en la γ-carboxilación de los factores de coagulación II, VII, IX y X, así como de la proteína C y S. Los niveles bajos de esta vitamina generan una actividad inadecuada de los factores de coagulación incrementando el riesgo de sangrado en diversos órganos, incluido el sistema nervioso central.
Los recién nacidos a término tienen el nivel de vitamina K un 50% menor que el de los adultos (2). Existen diferentes factores que contribuyen a que el recién nacido tenga depósitos bajos de vitamina K como lo son: el poco paso a través de la placenta, los escasos aportes que se reciben a través de la leche materna en niños con lactancia materna exclusiva y la ausencia de microflora intestinal productora de vitamina K como el Bacteroides fragilis (3,4).
La EHRN, según la edad de inicio, se clasifica en tres grupos (5):
- Precoz (<24 horas): se relaciona con el paso placentario de medicamentos maternos que inhiben la actividad de la vitamina K (ej. warfarina, fenitoína y fármacos tuberculostáticos como rifampicina e isoniacida). No se previene con la administración de vitamina K al nacimiento. Los sitios más frecuentes de sangrado son intratorácico, abdominal, umbilical y menos frecuentemente craneal.
- Clásica (1-7 días): asociada con aportes bajos de vitamina K. Se previene con la profilaxis al nacimiento. Aparece sangrado a nivel gastrointestinal, cutáneo, umbilical y con menos frecuencia intracraneal.
- Tardía (1 semana – 6 meses): ocurre principalmente en recién nacidos con lactancia materna exclusiva que no han recibido profilaxis con vitamina K o que se ha administrado de forma incorrecta. Menos frecuentemente se asocia a recién nacidos con problemas de malabsorción intestinal (fibrosis quística, atresia biliar, fallo hepático). Su manifestación más frecuente es la hemorragia intracraneal (50%) (6) así como sangrado cutáneo y gastrointestinal.
La incidencia de EHRN en los recién nacidos sin profilaxis es de 0,25-1,7% (7). Una revisión sistemática reciente muestra que, en ausencia de profilaxis, la frecuencia de la presentación tardía es de 35 (10,5-80) por cada 100000 recién nacidos vivos (3).
Desde la introducción de la profilaxis con vitamina K, la EHRN ha disminuido de forma significativa. Los datos epidemiológicos han mostrado que la profilaxis previene la incidencia de EHRN en sus presentaciones clásicas y tardías con una incidencia en la actualidad < 0,2/100 000 recién nacidos vivos (8,9). Los casos que siguen existiendo se presentan, en su mayoría, en recién nacidos alimentados con lactancia materna que no han recibido correctamente la profilaxis o en aquellos con déficits malabsortivos o hepatobiliares no diagnosticados (4). El riesgo relativo de desarrollar la forma tardía de EHRN es 81 veces mayor entre los recién nacidos que no reciben vitamina K intramuscular que aquellos que sí la reciben (10).
La adherencia a los programas de profilaxis con vitamina K, no está del todo bien documentada entre los diferentes países. En países como Nueva Zelanda y Australia, se ha registrado una tasa de rechazo de la profilaxis de un 1,7% y 1,2% respectivamente (11). Recientemente, se dispone de datos indirectos que sugieren que el número de padres que rechazan la profilaxis se está incrementando. En Estados Unidos se ha llegado a documentar una tasa de rechazo de 3,4% en el Hospital Universitario de Tennessee y de hasta un 28% en centros privados de la misma área (12).
Desde los años 60 la Academia Americana de Pediatría recomienda la administración de vitamina K (1 mg) intramuscular al nacimiento. Esta recomendación ha sido ratificada en 2022(13) y ha sido adoptada de forma global por diferentes países. Los Estándares Europeos para el Cuidado de los Recién Nacidos incluyen la profilaxis con vitamina K para prevenir la EHRN (14). En España la recomendación de profilaxis se encuentra vigente y recogida en la última guía nacional del Ministerio de Sanidad “Cuidados desde el nacimiento” (15).
MAGNITUD DEL PROBLEMA
Como se ha comentado previamente, el número de padres que rechazan la administración de vitamina K al nacimiento ha aumentado en los últimos años, situándose en 0,3% en Canadá (16), 1,7% en Nueva Zelanda y entre un 0,8-2,3% en Estados Unidos (11,12). Se estima que en EE.UU. aproximadamente 24 000 recién nacidos al año no reciben la profilaxis con vitamina K y esto genera unos 400 casos anuales de EHRN tardía (17).
En un estudio de la red pediátrica de vigilancia australiana, en el que recogen los casos de EHRN tardía de los últimos 24 años, se informa de un incremento de más del 50% en la proporción de padres que rechazan la administración de vitamina K en los últimos 6 años (18).
Considerando que la hemorragia intracraneal es el sangrado más frecuente en los casos de EHRN tardía, que genera una mortalidad entre el 14%–25% y trastornos en el neurodesarrollo en un 40%-67% (3,19), el rechazo parental a la profilaxis con vitamina K podría considerarse un problema de salud pública.
La no administración de vitamina K al nacimiento puede asociar otro tipo de conductas que suponen un riesgo para el recién nacido, como son el rechazo de la profilaxis ocular y el no inicio de los esquemas de vacunación. Se ha descrito que cuando los padres rechazan la administración de vitamina K, el riesgo relativo (RR) para rechazar también la vacunación es de 14,6 (IC 95% 13,9 – 15,3) (16).
MARCO ANALÍTICO
Traducción autorizada de: USPSTF Procedure Manual (Version 2). Rockville, MD: US. Preventive Services Task Force. December 2015. Available at USPSTF “Methods and Processes”, (https://www.uspreventiveservicestaskforce.org/uspstf/methods-and-proces…). Current as of March 2017.
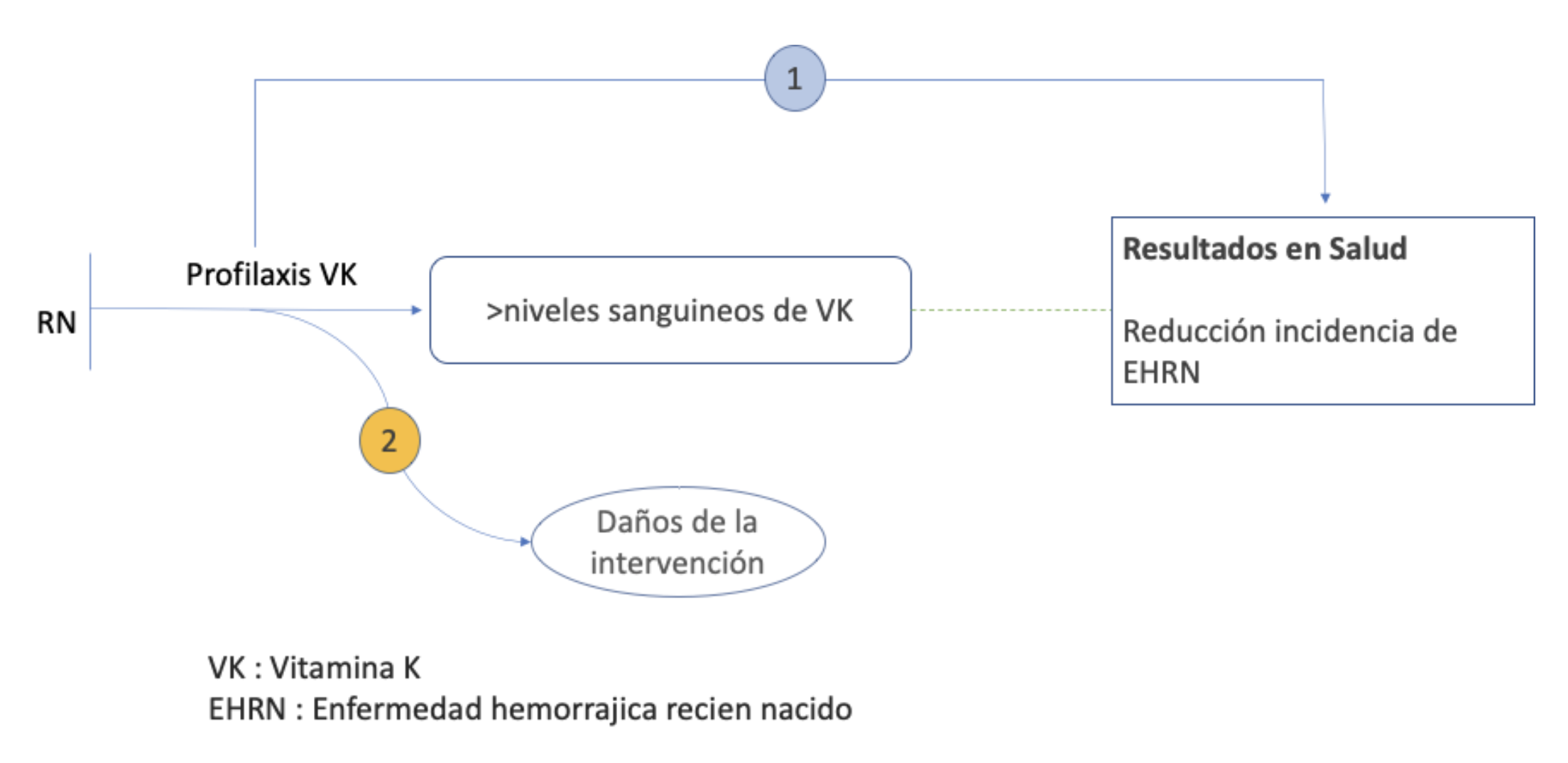
PREGUNTAS DERIVADAS DEL MARCO ANALÍTICO
1. ¿La profilaxis al nacimiento con vitamina K disminuye la incidencia de la enfermedad hemorrágica del recién nacido?
Clásica
En cuanto a la presentación clásica de la EHRN, en 3 revisiones sistemáticas de la literatura (3,20,21) se incluyen 2 ensayos clínicos aleatorizados en los que se encuentra una reducción de la EHRN en los grupos que recibieron la vitamina K. En el primero se evalúa la presencia de sangrado clínico desde el nacimiento hasta el séptimo día de vida en un grupo de niños que recibe profilaxis con vitamina K con otro grupo que no la recibe y se muestra que la administración de vitamina K reduce significativamente el riesgo de sangrado [RR 0,73 (0,56-0,96)] (22). El segundo evalúa la presencia de sangrado post circuncisión en 2 grupos (placebo vs 5 mg de vitamina K), de nuevo en el grupo que recibió profilaxis con vitamina K el riesgo de sangrado fue menor [RR 0,18 (0,08-0,42)] (23).
Una revisión Cochrane del año 2000, recoge además 11 estudios en los que se estudia la eficacia de la administración de vitamina K en los marcadores analíticos (PIVKA II y concentración plasmática de vitamina K) y se muestra cómo la administración de 1mg de vitamina K mejora los parámetros analíticos implicados en la EHRN y por tanto indirectamente concluye que la profilaxis es efectiva para prevenir EHRN clásica.
Tardía
No se han realizado ensayos clínicos para evaluar si la administración de vitamina K oral o intramuscular previene la EHRN tardía. En una revisión sistemática realizada por Sankar (3) se recogen dos estudios, en los que se analizan los casos reportados de EHRN tardía en Reino Unido y Alemania en los años 90, en ambos estudios se encuentra que la mayoría de los recién nacidos afectados de EHRN tardía no habían recibido la profilaxis al nacimiento con vitamina K. En el primero, realizado por McNinch (10), se recogieron las datos con respecto a casos de EHRN tardía y profilaxis con vitamina K en un periodo de 2 años en Inglaterra, encontraron un RR 0,01 (IC 95% 0,001–0,21) de EHRN tardía, al comparar los RN con profilaxis IM vs no profilaxis, y un RR 0,35 (IC 95% 0,13–0,93) al comparar la profilaxis oral vs no profilaxis. En el segundo, Von Kries (24) recoge los casos de EHRN tardía y su tipo de profilaxis a través de una encuesta a los hospitales de Alemania oriental, al comparar la profilaxis IM o SC vs no profilaxis, se encontraron resultados similares [RR 0,03 (IC 95% 0,004–0,25)] y al comparar oral vs no profilaxis [RR 0,2 (IC 95% 0,04–0,91)]. En la revisión de Sankar, los autores realizan un análisis agrupado de estos dos estudios, en el que se demuestra una disminución significativa en la incidencia de EHRN tardía al administrar profilaxis con vitamina K [RR 0,02 (IC 95% 0,00-0,10)].
La Sociedad Europea Pediátrica de Gastroenterología, Hepatología y Nutrición (ESPGHAN) en su última guía de consenso del 2016 sobre la prevención de la EHRN menciona que el seguimiento epidemiológico realizado por diferentes países ha demostrado que la política de profilaxis al nacimiento con vitamina K previene la EHRN en sus formas clásica y tardía (1).
No se han encontrado ensayos clínicos aleatorizados posteriores que comparen la administración de vitamina K con placebo, dado que, no sería ético llevar a cabo estudios que expongan a recién nacidos sanos a no recibir la profilaxis universal cuando se ha demostrado a través de otro tipo de estudios clínicos que su administración previene la EHRN en su forma clásica y tardía.
2. ¿La profilaxis con vitamina K al nacer produce daños?
En la década de los 90 se relacionó la profilaxis con vitamina K con un incremento en el riesgo de cáncer en la infancia. La Organización Mundial de la Salud (OMS) en el año 1999 hizo una revisión de la literatura en la que concluyó que no existe evidencia sobre el perfil cancerígeno de la vitamina K (11). La Academia Americana de Pediatría en el año 2003, tras revisar los datos que suscitaron dicha relación, concluyó que no existe asociación entre la administración de vitamina K y leucemia y cáncer en el periodo infantil y recomienda su uso en los recién nacidos tras el parto (7).
Uno de los efectos adversos de la profilaxis intramuscular con vitamina K es el dolor. Al igual que en la administración de otras profilaxis, la vitamina K se debería administrar con medidas no farmacológicas para prevenir y disminuir el dolor como son el amamantamiento, la administración de sacarosa, la contención etc. (25).
Como ya se ha mencionado, la administración oral tiene desventajas, ya que exige un estricto cumplimiento por parte de los padres durante varias semanas. El insuficiente cumplimiento se ha asociado con un incremento en el riesgo de EHRN (8,26).
OTRAS PREGUNTAS
¿Los beneficios de la administración de vitamina K como profilaxis al nacimiento difiere según la vía de administración (oral, intramuscular, intravenosa)?
Oral versus intramuscular
Según los datos de seguimiento de diferentes países que usan la vía oral para la administración de la profilaxis con vitamina K, la vía oral es una opción terapéutica efectiva para prevenir la EHRN, sin embargo, la incidencia de EHRN en estas series es mayor que las reportadas por países que usan la vía intramuscular (27,28). Australia, al cambiar la vía de administración oral por la intramuscular redujo en más de la mitad la incidencia de EHRN en general y específicamente la forma tardía (18).
Dado el aumento de la frecuencia de EHRN, especialmente en recién nacidos con alto riesgo de colestasis biliar no diagnosticados al nacimiento (29), Holanda cambió la pauta de administración de la vitamina K en los recién nacidos con lactancia materna exclusiva (1 mg oral al nacimiento, seguido de 25 mcg/día hasta la semana 13) incrementando la dosis de mantenimiento a 150 mcg/día desde la semana 8 a la semana 13 (30). Por su parte, Dinamarca hasta el año 2000 recomendaba administrar 2 mg de vitamina K por vía oral al nacimiento seguido de 1 mg/semana durante 3 meses. Tras una revisión de la evidencia disponible cambió la recomendación y pasó a administrar 1 mg por vía intramuscular al considerar que ofrecía mayor protección contra la EHRN.
No se ha comparado por medio de ensayos clínicos aleatorizados el efecto de una dosis única de vitamina K IM frente a dosis repetidas de vitamina K oral para la prevención de EHRN tardía.
Cabe destacar que, actualmente existe gran variabilidad en la dosificación por vía oral entre países, y que el adecuado cumplimiento de la pauta por parte de los padres es la que garantiza la efectividad de esta medida preventiva. En los casos de EHRN en recién nacidos que han recibido la profilaxis oral se han detectado pautas incorrectas de administración.
Aunque las recomendaciones Holandesas (30) hacen hincapié en la dosificación oral en RN con lactancia materna exclusiva, en otros países como Francia (31) la salvedad según el modo de alimentación no está claramente contemplada. Los principales inconvenientes de la profilaxis oral además del cumplimiento en domicilio, es la variabilidad de absorción entre individuos, y el acceso a la formulación oral especialmente en población vulnerable. En las recomendaciones más recientes por parte de los Estándares Europeos para el Cuidado de los Recién Nacidos (13) y de la ESPGHAN (1) no se diferencia la dosificación oral según la forma de alimentación.
| Esquema de administración |
País |
Nº niños |
Incidencia/100000 |
Oral
3 dosis de 2 mg (postnatal, entre el 3-10 día y entre la semana 4-6) |
Alemania (32) |
1817769 |
0.73 (IC 0.23-2.2) |
| |
Suiza (33) |
458184 |
0.0 (IC 0.0-0,81) |
| |
Total |
2275953 |
0.35 (IC 0.16-0.69) |
Oral
3 dosis de 2 mg (postnatal, entre el 3-4 día y en el 1r mes de vida) |
Francia (31)
(Desde 2017) |
-- |
No datos disponibles |
Oral
1mg postnatal, entre el día 1-8 25 mcg/día, entre los 8 días-12 semanas 150 mcg/día |
Holanda (30)
(Desde 2011) |
-- |
No datos disponibles |
Oral
Enero 1993-marzo 1994 |
Australia (18) |
325203 |
Total 2,46 (1.06-4.85)
Tardía 1.85 (0.68-4.02) |
Intramuscular
1 mg IM desde 1994 |
Australia |
6584775 |
Total 0.76 (0.56 – 1)
Tardía 0.5 (0.38-0.76) |
| |
Total |
6909978 |
Total 0.84 (0.64 – 1.08)
Tardía 0.61 (0.44-0.82) |
Intramuscular
1 mg |
NZ (9) |
654000 |
0.16 (0-0.46) |
Intramuscular
1 mg aunque incluye datos de pauta oral |
UK (26) |
1700000 |
0.24 (0.0 -0.35) |
| |
TOTAL |
2354000 |
0.21 (0.06-0.5) |
Tabla 1. Pautas de administración de vitamina K por países e Incidencia de EHRN. Adaptación y traducción de Prevention of Vitamin K Deficiency Bleeding in Newborn Infants: A Position Paper by the ESPGHAN Committee on Nutrition. (1) NZ: Nueva Zelanda UK: Reino Unido.
Intravenosa
Al administrar por vía intravenosa la vitamina K existe una mayor excreción urinaria de sus metabolitos, lo que implicaría una menor capacidad de depósito en los tejidos perdiendo con el tiempo su capacidad de liberación en la circulación sistémica. Por este motivo, para prevenir la EHRN, se prefiere la vía intramuscular a la intravenosa, reservando esta última para recién nacidos a término o pretérmino graves, o recién nacidos con patología colestática (1,34).
¿La profilaxis con vitamina K en recién nacidos prematuros para prevenir la EHRN difiere de la de los recién nacidos a término?
Los recién nacidos prematuros y especialmente los de muy bajo peso, tienen un incremento en el riesgo de déficit de vitamina K dada su inmadurez hepática y el retraso en la colonización intestinal por la microflora, así como por la exposición a antibioterapia que modifica la microbiota.
Existen pocos estudios que evalúen los efectos de la vitamina K en recién nacidos prematuros, y también existe gran variabilidad en las pautas de dosificación entre unidades (35). Las publicaciones disponibles sugieren que esta población puede tener niveles de vitamina K tras la profilaxis más elevados que los recién nacidos a término.
La última revisión Cochrane (36) incluye un ensayo clínico(37) en el que se aleatorizan recién nacidos prematuros menores de 32 semanas de edad gestacional a recibir una de tres pautas de profilaxis (0,5 mg IM, 0,2 mg IM, 0,2 mg IV). Se estudiaron los cambios en los parámetros bioquímicos relacionados con la vitamina K al nacimiento, a los 5 días de vida y a las 2 semanas de alcanzar aportes enterales completos. A los 5 días de vida, los recién nacidos en los tres grupos estudiados tenían niveles suprafisiológicos de vitamina K, sin embargo, en el día 25 los niveles habían disminuido en los tres grupos siendo más marcado en el grupo que recibió la profilaxis por vía intravenosa.
Los autores de la revisión Cochrane consideran prudente continuar la profilaxis con vitamina K en los recién nacidos prematuros, pero faltan estudios con respecto a la dosis y vía de administración apropiada. Por su parte, la Sociedad Pediátrica de Canadá en su último consenso recomienda administrar una dosis de vitamina K intramuscular de 0.5 mg para recién nacidos con peso al nacimiento <1500 g y de 1 mg para los > 1500 g. Advierten que la profilaxis intravenosa con 0.2 mg puede no ser tan eficaz en prevenir la EHRN, y dada la baja evidencia no recomiendan la administración intravenosa en este grupo poblacional (38). La última actualización de la Academia Americana de Pediatría coincide con las recomendaciones del grupo canadiense, aunque mantienen como posible dosificación para <1500 g una dosis intramuscular entre 0,3mg/kg y 0,5 mg/kg. También advierten que la administración intravenosa en este grupo poblacional no está recomendada. (13)
En los Estándares Europeos para el Cuidado del Recién Nacido (EFCNI) con respecto a la profilaxis en prematuros, resaltan que pueden ser necesarias dosis menores de vitamina K, proponiendo administrar 0,5 mg para recién nacidos con peso >1000 gramos o 0,2 mg para aquellos con peso <1000 g por vía intramuscular o intravenosa (14).
SÍNTESIS DE LA EVIDENCIA
En el año 2000 tras una revisión sistemática de la literatura, el grupo Cochrane concluyó que la profilaxis al nacimiento con vitamina K previene la EHRN en su presentación clásica. (21) Sin embargo, con respecto a la presentación tardía no existen ensayos clínicos aleatorizados publicados; se debe tener en cuenta que su realización sería poco factible ya que al ser una entidad poco frecuente se necesitaría un tamaño poblacional muy grande y conllevaría altas implicaciones éticas, debido a que existen otro tipo de estudios en la literatura que permiten evaluar el efecto de la profilaxis en la presentación tardía de la enfermedad. A través del seguimiento epidemiológico en distintos países se ha demostrado que la administración de vitamina K al nacimiento previene también la EHRN en su forma tardía (1,8,9,39).
Los efectos adversos derivados de la profilaxis son leves y poco frecuentes, el dolor secundario a la administración intramuscular puede disminuirse a través de medidas no farmacológicas (40).
La EHRN es una enfermedad grave. Hay buena evidencia de que la administración de vitamina K en el RN es segura y eficaz, los daños potenciales son leves, por lo que está claro el beneficio neto a favor de la administración.
RECOMENDACIONES DE OTROS GRUPOS
Los Estándares Europeos para el cuidado de los Recién Nacidos (EFCNI) (14), la Sociedad Canadiense de Pediatría (38), la Academia Americana de Pediatría (7,13), la Sociedad Europea Pediátrica de Gastroenterología, Hepatología y Nutrición (ESPGHAN) (1) y la guía del Instituto Nacional de Salud Británico (NICE) (41) recomiendan la profilaxis universal con 1 mg de vitamina K al nacimiento por vía intramuscular. Aunque los Estándares Europeos y la ESPGHAN incluyen la posibilidad de dosificaciones orales, las otras sociedades reservan las formulaciones orales para padres que rechazan la vía intramuscular, sin embargo, todas coinciden en indicar que la vía intramuscular es la más eficaz como actividad preventiva.
RECOMENDACIONES DE PREVINFAD
- Después del nacimiento se recomienda administrar a todos los recién nacidos 1 mg de vitamina K de forma profiláctica por vía intramuscular para prevenir la EHRN (fuerte a favor)
- Consideraciones especiales:
- Con respecto a los niños prematuros:
- Si el peso al nacimiento es menor de 1500 g: se sugiere administrar 0,5 mg en vez de 1 mg de vitamina K. Se administrará preferiblemente vía IM.
- Se sugiere administrar la vitamina K vía intravenosa en recién nacidos graves (término y pretérmino), que corren riesgo de inestabilizarse por la administración intramuscular y para aquellos recién nacidos con enfermedad colestática conocida.
- Si los padres rechazan la profilaxis intramuscular:
- Se recomienda la siguiente pauta oral: Tres dosis de 2 mg de vitamina K oral (al nacimiento, entre el cuarto y el sexto día de vida, y entre las cuatro y seis semanas de vida).
PROPUESTA OPERATIVA
- Se debe informar a los padres de que se va a administrar la vitamina K.
- No se administrará inmediatamente tras el nacimiento, sino que se respetará el tiempo de contacto piel con piel con su madre (al menos 50 minutos). No está justificado separar al recién nacido sólo para administrarle la vitamina K.
- Cuando se administre la vitamina K, si se puede, el niño estará al pecho de su madre por el efecto analgésico del amamantamiento. Si no se puede poner al pecho para la administración, se puede administrar entre 0,2-0,5 ml de sacarosa al 20%, dos minutos antes de la inyección y se le ofrecerá una tetina para succionar.
- Padres que rechazan a la administración:
- Si los padres rechazan la vitamina K IM se les ofrecerá la pauta oral (tres dosis de 2 mg de vitamina K oral, al nacimiento, entre el cuarto y el sexto día de vida, y entre las cuatro y seis semanas de vida). Se les insistirá en la importancia del cumplimiento, sobre todo si tiene además algún factor de riesgo, prematuridad, trauma de parto, madre que haya tomado antiepilépticos, patología hepática. Se reflejará esta pauta en la cartilla de salud y en el informe de alta, así como se notificará a su centro de salud para hacer seguimiento de la profilaxis.
- Si los padres se niegan a la profilaxis, un neonatólogo experimentado les explicará los riesgos reales de la ausencia de profilaxis y se les informará que existen pruebas científicas de buena calidad que justifican la profilaxis porque se evitan muertes y secuelas. Se registrará la información en la historia clínica.
- A los niños prematuros si el peso al nacimiento es menor de 1.500 g: administrar 0,5 mg IM o IV.
- A los niños que ingresen en cuidados intermedios o UCI, salvo que estén inestables, se recomienda administrar la profilaxis por vía intramuscular.
INFORMACIÓN A LOS PADRES SOBRE LA PROFILAXIS CON VITAMINA K
Información prenatal
Durante la preparación al parto y en las visitas de seguimiento del embarazo, se deben “normalizar” todas las actividades preventivas del recién nacido e incluirlas en el plan de parto. A los padres que se muestren con dudas con respecto a alguna de las actividades preventivas se recomienda que sean aconsejados por un pediatra o neonatólogo (ver siguiente apartado).
Información periparto
Si antes del parto o en el momento de administrar la profilaxis los padres manifiestan que no desean administrar la profilaxis al recién nacido, un profesional (pediatra o neonatólogo) abordará con los padres los motivos por los que no desean la profilaxis. Se recomienda iniciar la conversación permitiendo que los padres manifiesten en primer lugar sus dudas y preocupaciones, los conocimientos que tienen al respecto y cuál ha sido el proceso de toma de decisión. Esto permitirá ofrecer opciones con las que los padres se sientan cómodos. Los profesionales deben abogar por las medidas para preservar el mejor interés del recién nacido (42).
Se han identificado algunos motivos para rechazar la vitamina K, y se proponen algunas estrategias para abordarlas:
- Preocupación por el riesgo de leucemia: Como se ha comentado previamente, no se ha demostrado en estudios posteriores la relación entre la administración de vitamina K con leucemia o cáncer en la infancia.
Los padres pueden percibir un riesgo mayor por los efectos adversos de la profilaxis que el riesgo de EHRN como tal. Por esto es importante destacar que la no profilaxis conlleva un riesgo aún mayor de enfermedad hemorrágica del recién nacido con posibles secuelas graves. (42,43) El abordaje propuesto para padres que rechazan vacunas y que podría ser extrapolable a otras actividades preventivas, sugiere optar por un discurso narrativo desde experiencias personales más que ofrecer datos estadísticos (17). Más que dar a los padres la frecuencia de EHRN se les puede decir que el riesgo de padecerla es 80 veces mayor si no se administra la profilaxis con vitamina K.
- Preocupación por el dolor en el recién nacido: la administración intramuscular es un procedimiento doloroso para el recién nacido, por este motivo se recomienda no administrar inmediatamente tras el nacimiento, respetando el contacto piel con piel, y administrarla durante el amamantamiento por el efecto analgésico (40,44). Si no se puede poner al pecho para la administración, se puede administrar entre 0,2-0,5 ml de sacarosa al 20%, dos minutos antes de la inyección y se le ofrecerá una tetina para succionar (45).
- Dieta materna rica en vitamina K: las familias que desean lactancia materna exclusiva pueden decidir incrementar los aportes maternos de vitamina K con el fin de aportar más vitamina K a través de la leche materna, sin embargo, el paso a través de la leche materna es bajo incluso en mujeres con aportes orales altos (46,47).
- Algunas familias tienden a decidir intervenciones “naturales”, en un esfuerzo para no medicalizar un proceso natural como es el parto. La administración de la profilaxis se puede enfocar desde el punto de vista “la vitamina K es un cuidado para que los bebés sanos se mantengan sanos” (43,48)
Aunque la eficacia de la profilaxis oral es menor que la intramuscular, si los padres siguen rechazando la administración intramuscular, se les ofrecerá la posibilidad de la administración oral insistiendo en la importancia de su cumplimiento estricto. Si es posible se podría notificar a Atención Primaria para que desde allí se apoye el cumplimiento de la administración oral de la vitamina K (ver apartado de recomendaciones). En España los padres no tienen la obligación de aceptar para sus hijos las intervenciones profilácticas por ello no tiene sentido llamar al juez para comunicar que los padres se niegan a que el recién nacido reciba la vitamina K.
ESTRATEGIA DE BÚSQUEDA
Palabras clave:
- Descriptores MESH: vitamin K; Vitamin K Deficiency Bleeding.
Bases de datos:
- MEDLINE/PubMed; Embase.
- IME.
Estrategia de búsqueda en MedLine:
- (("vitamin K"[Mesh]) AND ("infant,newborn"[Mesh])
- (("vitamin K"[Mesh]) AND (“infant,newborn"[Mesh]) AND ("prophylaxis"[Mesh])
- (("Vitamin K Deficiency Bleeding"[Mesh] AND ("infant,Newborn"[Mesh] OR "infant,newborn"[Mesh])
Bibliotecas:
- Cochrane Library/Biblioteca Cochrane Plus, Trip Database, BVS, SciELO, NICE, EFCNI.
BIBLIOGRAFÍA
- Mihatsch WA, Braegger C, Bronsky J, Campoy C, Domellöf M, Fewtrell M, et al. Prevention of Vitamin K Deficiency Bleeding in Newborn Infants: A Position Paper by the ESPGHAN Committee on Nutrition. Journal of Pediatric Gastroenterology and Nutrition. 2016 Jul;63(1):123–9.
- Pichler E, Pichler L. The neonatal coagulation system and the vitamin K deficiency bleeding - a mini review. Wien Med Wochenschr. 2008;158(13–14):385–95.
- Sankar MJ, Chandrasekaran A, Kumar P, Thukral A, Agarwal R, Paul VK. Vitamin K prophylaxis for prevention of vitamin K deficiency bleeding: a systematic review. Journal of Perinatology. 2016 May;36(S1):S29–35.
- Saxonhouse MA. Neonatal Bleeding and Thrombotic Disorders. In: Avery’s diseases of the newborn. 10th ed. Philadelphia: ELSEVIER; 2018. p. 1121–38.
- Sutor AH, von Kries R, Cornelissen EA, McNinch AW, Andrew M. Vitamin K deficiency bleeding (VKDB) in infancy. ISTH Pediatric/Perinatal Subcommittee. International Society on Thrombosis and Haemostasis. Thromb Haemost. 1999 Mar;81(3):456–61.
- Miyasaka M, Nosaka S, Sakai H, Tsutsumi Y, Kitamura M, Miyazaki O, et al. Vitamin K deficiency bleeding with intracranial hemorrhage: focus on secondary form. Emerg Radiol. 2007 Oct;14(5):323–9.
- Committee on Fetus and Newborn. Controversies Concerning Vitamin K and the Newborn. PEDIATRICS. 2003 Jul 1;112(1):191–2.
- McNinch A, Busfield A, Tripp J. Vitamin K deficiency bleeding in Great Britain and Ireland: British Paediatric Surveillance Unit Surveys, 1993 94 and 2001-02. Arch Dis Child. 2007 Sep;92(9):759–66.
- Darlow BA, Phillips AA, Dickson NP. New Zealand surveillance of neonatal vitamin K deficiency bleeding (VKDB): 1998-2008. J Paediatr Child Health. 2011 Jul;47(7):460–4.
- McNinch AW, Tripp JH. Haemorrhagic disease of the newborn in the British Isles: two year prospective study. BMJ. 1991 Nov 2;303(6810):1105–9.
- Majid A, Blackwell M, Broadbent RS, Barker DP, Al-Sallami HS, Edmonds L, et al. Newborn Vitamin K Prophylaxis: A Historical Perspective to Understand Modern Barriers to Uptake. Hosp Pediatr. 2019;9(1):55–60.
- Warren M, Miller A, Traylor J, Sidonio R, Morad A, Goodman A, et al. Late Vitamin K Deficiency Bleeding in Infants Whose Parents Declined Vitamin K Prophylaxis — Tennessee, 2013. MMWR Morb Mortal Wkly Rep. 2013 Nov 15;62(45):901–2.
- Hand I, Noble L, Abrams SA. Vitamin K and the Newborn Infant. Pediatrics. 2022 Mar 1;149(3):e2021056036.
- EFCNI, Koletzko B, Buonocore G, et al. Prevention of vitamin K deficiency bleeding (VKDB) at birth. In: European Standards of Care for Newborn Health [Internet]. 2018 [cited 2020 Aug 5]. Available from: https://newborn-health-standards.org/prevention-vkdb/
- Grupo Prevención en la Infancia y Adolescencia de la Asociación Española de Pediatría de Atención Primaria. Uso profiláctico de la vitamina K para la enfermedad hemorrágica del recién nacido. In: Cuidados desde el nacimiento Recomendaciones basadas en pruebas y buenas prácticas. Ministerio de Sanidad y Política Social; 2010. p. 58–63.
- Sahni V, Lai FY, MacDonald SE. Neonatal Vitamin K Refusal and Nonimmunization. PEDIATRICS. 2014 Sep 1;134(3):497–503.
- Shah SI, Brumberg HL, La Gamma EF. Applying lessons from vaccination hesitancy to address birth dose Vitamin K refusal: Where has the trust gone? Seminars in Perinatology. 2020 Jun;44(4):151242.
- Zurynski Y, Grover CJ, Jalaludin B, Elliott EJ. Vitamin K deficiency bleeding in Australian infants 1993–2017: an Australian Paediatric Surveillance Unit study. Archives of Disease in Childhood. 2020 May;105(5):433–8.
- Schulte R, Jordan LC, Morad A, Naftel RP, Wellons JC, Sidonio R. Rise in Late Onset Vitamin K Deficiency Bleeding in Young Infants Because of Omission or Refusal of Prophylaxis at Birth. Pediatric Neurology. 2014 Jun;50(6):564–8.
- Martín-López JE, Carlos-Gil AM, Rodríguez-López R, Villegas-Portero R, Luque-Romero L, Flores-Moreno S. La vitamina K como profilaxis para la enfermedad hemorrágica del recién nacido. Farmacia Hospitalaria. 2011 May;35(3):148–55.
- Puckett RM, Offringa M. Prophylactic vitamin K for vitamin K deficiency bleeding in neonates. Cochrane Neonatal Group, editor. Cochrane Database of Systematic Reviews [Internet]. 2000 Oct 23 [cited 2020 Jul 14]; Available from: http://doi.wiley.com/10.1002/14651858.CD002776
- Sutherland JM, Glueck HI, Gleser G. Hemorrhagic disease of the newborn. Breast feeding as a necessary factor in the pathogenesis. Am J Dis Child. 1967 May;113(5):524–33.
- Vietti TJ, Murphy TP, James JA, Pritchard JA. Observations on the prophylactic use of vitamin K in the newborn infant. The Journal of Pediatrics. 1960 Mar 1;56(3):343–6.
- von Kries R. Vitamin K prophylaxis--a useful public health measure? Paediatr Perinat Epidemiol. 1992 Jan;6(1):7–13.
- Pallás‐Alonso CR. Uso profiláctico de la vitamina k para la enfermedad hemorrágica del recién nacido | Previnfad [Internet]. Recomendaciones PrevInfad / PAPPS [en línea]. 2010 [cited 2020 Jul 27]. Available from: http://previnfad.aepap.org/monografia/vitamina-k
- Busfield A, Samuel R, McNinch A, Tripp JH. Vitamin K deficiency bleeding after NICE guidance and withdrawal of Konakion Neonatal: British Paediatric Surveillance Unit study, 2006-2008. Arch Dis Child. 2013 Jan;98(1):41–7.
- von Kries R, Hachmeister A, Göbel U. Can 3 oral 2 mg doses of vitamin K effectively prevent late vitamin K deficiency bleeding? Eur J Pediatr. 1999 Dec;158 Suppl 3:S183-186.
- Schubiger G, Berger TM, Weber R, Bänziger O, Laubscher B, Swiss Paediatric Surveillance Unit. Prevention of vitamin K deficiency bleeding with oral mixed micellar phylloquinone: results of a 6-year surveillance in Switzerland. Eur J Pediatr. 2003 Dec;162(12):885–8.
- van Hasselt PM, de Koning TJ, Kvist N, de Vries E, Lundin CR, Berger R, et al. Prevention of vitamin K deficiency bleeding in breastfed infants: lessons from the Dutch and Danish biliary atresia registries. Pediatrics. 2008 Apr;121(4):e857-863.
- de Winter JP, Joosten KFM, Ijland MM, Verkade HJ, Offringa M, Dorrius MD, et al. [New Dutch practice guideline for administration of vitamin K to full-term newborns]. Ned Tijdschr Geneeskd. 2011;155(18):A936.
- Hascoët JM, Picaud JC, Lapillonne A, Boithias-Guerot C, Bolot P, Saliba E. Vitamine K chez le nouveau-né : mise à jour des recommandations. Archives de Pédiatrie. 2017 Sep;24(9):902–5.
- von Kries R, Hachmeister A, Göbel U. Oral mixed micellar vitamin K for prevention of late vitamin K deficiency bleeding. Arch Dis Child Fetal Neonatal Ed. 2003 Mar;88(2):F109-112.
- Laubscher B, Bänziger O, Schubiger G, Swiss Paediatric Surveillance Unit (SPSU). Prevention of vitamin K deficiency bleeding with three oral mixed micellar phylloquinone doses: results of a 6-year (2005-2011) surveillance in Switzerland. Eur J Pediatr. 2013 Mar;172(3):357–60.
- Harrington DJ, Clarke P, Card DJ, Mitchell SJ, Shearer MJ. Urinary Excretion of Vitamin K Metabolites in Term and Preterm Infants: Relationship to Vitamin K Status and Prophylaxis. Pediatric Research. 2010 Dec;68(6):508–12.
- Clarke P, Mitchell S. Vitamin K prophylaxis in preterm infants: current practices. Journal of Thrombosis and Haemostasis. 2003 Feb;1(2):384–6.
- Ardell S, Offringa M, Ovelman C, Soll R. Prophylactic vitamin K for the prevention of vitamin K deficiency bleeding in preterm neonates. Cochrane Neonatal Group, editor. Cochrane Database of Systematic Reviews [Internet]. 2018 Feb 5 [cited 2020 Mar 15]; Available from: http://doi.wiley.com/10.1002/14651858.CD008342.pub2
- Clarke P, Mitchell SJ, Wynn R, Sundaram S, Speed V, Gardener E, et al. Vitamin K Prophylaxis for Preterm Infants: A Randomized, Controlled Trial of 3 Regimens. PEDIATRICS. 2006 Dec 1;118(6):e1657–66.
- Ng E, Loewy AD. Position Statement: Guidelines for vitamin K prophylaxis in newborns. Can Fam Physician. 2018 Oct;64(10):736–9.
- von Kries R, Hanawa Y. Neonatal vitamin K prophylaxis. Report of Scientific and Standardization Subcommittee on Perinatal Haemostasis. Thromb Haemost. 1993 Mar 1;69(3):293–5.
- Shah PS, Aliwalas LI, Shah V. Breastfeeding or breast milk for procedural pain in neonates. Cochrane Database Syst Rev. 2006 Jul 19;(3):CD004950.
- National Institute for Health and Care Excellence [NICE 2015)]. Postnatal care up to 8 weeks after birth. NICE guideline 37 [Internet]. 2015. Available from: www.nice.org.uk/guidance/cg37
- Kerruish NJ, McMillan J, Wheeler BJ. The ethics of parental refusal of newborn vitamin K prophylaxis: Ethics of parental refusal of vitamin K. Journal of Paediatrics and Child Health. 2017 Jan;53(1):8–11.
- Moses BD, Borecky AD, Dubov A. It is OK to nudge for vitamin K. Acta Paediatrica. 2019 Nov;108(11):1938–41.
- Shah PS, Aliwalas L, Shah V. Breastfeeding or breastmilk to alleviate procedural pain in neonates: a systematic review. Breastfeed Med. 2007 Jun;2(2):74–82.
- Stevens B, Yamada J, Ohlsson A, Haliburton S, Shorkey A. Sucrose for analgesia in newborn infants undergoing painful procedures. Cochrane Database Syst Rev. 2016 Jul 16;7:CD001069.
- Khambalia AZ, Roberts CL, Bowen JR, Nassar N. Maternal and infant characteristics by mode of vitamin K prophylaxis administration. J Paediatr Child Health. 2012 Aug;48(8):665–8.
- Greer FR. Vitamin K in human milk--still not enough. Acta Paediatr. 2004 Apr;93(4):449–50.
- Strehle E. New ways of preventing vitamin K deficiency bleeding in infancy. Acta Paediatrica. 2019 Nov;108(11):1936–7.
Las autoras declaran que no tienen conflictos de intereses en relación con el tema abordado en este documento.
Cómo citar este artículo: Morales C, Pallás CR. Uso profiláctico de la vitamina K para prevenir la enfermedad hemorrágica del recién nacido. PrevInfad/PAPPS [en línea]. Actualizado 6 de febrero de 2021. [consultado DD-MM-AAAA]. Disponible en http://previnfad.aepap.org/monografía/vitaminak